Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Ciencia, Tecnología e Innovación
versión impresa ISSN 2225-8787
Rev. Cien. Tec. In. vol.19 no.23 Chuquisaca jun. 2021
ARTICULO
CONSIDERACIONES FARMACOLÓGICAS Y DE PROPIEDAD INTELECTUAL PARA EL DESARROLLO DE MEDICAMENTOS USADOS EN EL TRATAMIENTO DE COVID-19
PHARMACOLOGICAL AND INTELLECTUAL PROPERTY CONSIDERATIONS FOR THE DEVELOPMENT OF DRUGS USED IN THE COVID-19 TREATMENT
Dr. Ramón Soto Vázquez*, David Aquino Guzmán*, Berenice Campos Castilla*, Luis Alan Cenobio Castillo*, Dra. Teresa Corona Ortega*, Dra. Patricia Parra Cervantes*, Eduardo Enrique Soto Parra **BrendaNaomi Torres Méndez*, Médico Luis Francisco Valdés Corona***.
*Facultad de Estudios Profesionales Zaragoza, de la Universidad Nacional Autónoma de México.*** Research Pro Laboratory Ciudad de México, México*** Medico Internista y traumatólogo egresado de la UNAM, Ciudad de México, México.ramonsv@unam.mx
Recibido enero 6, 2021; Aceptado abril 19, 2021
Resumen:
La infección por SARS-CoV-2 ha generado graves problemas de salud a la humanidad, por tratarse de una enfermedad infecciosa causada por un agente etiológico nuevo, por lo que aún no se tiene un tratamiento específico. Gracias a los esfuerzos en conjunto de toda la sociedad científica se ha logrado identificar el virus, su estructura genómica y el cómo se desarrolla la infección de la COVID-19 en los pacientes diagnosticados. Debido a la continua investigación, la industria farmacéutica ofrece moléculas cuya actividad farmacológica es parcialmente positiva no solo para el tratamiento de los principales síntomas en diferentes etapas de la infección de COVID-19, sino también para las complicaciones que suelen presentarse en lospacientes si es que se actúa de manera temprana. En este artículo se realiza una revisión de las moléculas más usadas para el tratamiento de COVID-19 con la finalidad de proporcionar una guía sobre la factibilidad de uso de las moléculas conocidas que se usan en dicha enfermedad, para ello se realizó la recopilación bibliográfica de la información disponible hasta ahora sobre lo que se conoce de COVID-19 y de los principios activos que actúan efectivamente. Se hace especial énfasis en las propiedades fisicoquímicas y la estructura de los principios activos para dar las pautas de posibles tratamientos en la infección por COVID-19; además, se incluye una revisión de opinión sobre las patentes relacionadas a los mencionados principios activos para resaltar la facilidad de su posible uso o modificación de sus formulaciones.
Palabras clave:
COVID-19, Patentes, Tratamientos, Genéricos, Biotecnológicos, SARS
ABSTRACT
The SARS-CoV-2 infection has generated serious health problems for humanity, as it is an infectious disease caused by a new etiological agent and there is still no a specific treatment. Thanks to the joint efforts of the entire scientific society, it has been possible to identify the virus, its genomic structure and how the COVID-19 infection develops in diagnosed patients. Due to continuous research, the pharmaceutical industry offers molecules whose pharmacological activity is partially positive not only for the main symptoms treatment at different stages of COVID-19 infection, but also for the complications occurred in patients, if treated early.
This article presents a review of the most used molecules for the COVID-19 treatment with the purpose of providing a guide on the use feasibility of the known-molecules that are used for this disease. This involves a consolidated bibliography of information available so far on what it is known about COVID-19 and the active ingredients that act effectively. Special emphasis is placed on the physicochemical properties and the activeingredients structure in terms of providing guidelines for possible treatments in COVID-19 infection. In addition, an opinion review on the patents related to the aforementioned active ingredients is included for highlighting the facility of their possible uses or modifications on their formulations.
Keyword:
Covid, Patents, Treatment, Generic, Biotech, SARS1.
1. Introducción
A finales de diciembre del 2019 en Wuhan, capital de la provincia de Hubei en China, surgieron casos de neumonía con signos clínicos similares a una neumonía viral, después de varias pruebas realizadas a los pacientes se identificó el virus SARS-CoV-2 como el causante de dicha afección. (Huang, C et al. 2020)
La Organización Mundial de la Salud (OMS) nombró el síndrome CoronaVirus Disease-2019 (COVID-19), y después fue renombrado como "Síndrome Respiratorio Agudo Severo" (SARS) Coronavirus (CoV) -2 (SARS-CoV-2) por el grupo de estudio de coronavirus del Comité Internacional de Taxonomía de Virus (Jiang S et al. 2020).
La epidemia de COVID-19 fue declarada por laOMS una emergencia de salud pública de preocupación internacional el 30 de enero de2020.
El 11 de marzo de 2020 en una conferencia de prensa el Director General de la Organización Mundial de la Salud, el Dr. Tedros Adhanom Ghebreyesus, declaró que la enfermedad por el coronavirus 2019 (COVID-19) era ya una pandemia. La caracterización de pandemia significa que la epidemia se ha extendido por varios países, continentes o todo el mundo, y que afecta a un gran número de personas. (en www.who.int/emergencies ).
Lo anterior ha causado que todo el mundo, se enfrente a una pandemia que ha cambiado completamente nuestro estilo de vida, pues esta nueva enfermedad continúa propagándose; razón por la cual, una revisión de los principales tratamientos farmacológicos, así como de las patentes que los protegen será de gran utilidad para el desarrollo de productos farmacéuticos y combatir esta infección para salvar vidas.
2. Estructura genómica de SARS-CoV-2
El SARS-CoV-2 pertenece al reino Riboviria, orden Nidovirales, suborden Cornidovirineae, familia Coronaviridae, subfamilia Orthocoronavirinae, género Betacoronavirus (linaje B), (Chan JF-W et al., 2020) subgénero Sarbecovirus y la especie Coronavirus que está relacionado con el síndrome respiratorio agudo severo. (Yoshimoto, F.K., 2020)
El genoma del SARS-CoV-2 codifica cuatro proteínas estructurales similares a otros coronavirus. (Yoshimoto, F.K., 2020):
S (espiga)
E (envoltura)
M (membrana)
N (nucleocápside)
La proteína S es responsable de la unión y entrada del SARS-CoV-2 al receptor de la célula objetivo del huésped, probablemente la enzima convertidora de angiotensina II (ACE2) expresada principalmente en las células epiteliales alveolares tipo II (AECII) (Xu,X et al., 2020) (Li, M et al. 2020)
3. Síntomas y diagnóstico de COVID-19
Es importante mencionar que no todas las personas expuestas al SARS-CoV-2 están infectadas y no todos los pacientes infectados desarrollan una enfermedad respiratoria grave. Sin embargo, la infección por SARS-CoV-2 se puede dividir en tres etapas (Shi Y. 2020):
1. Etapa I. Un periodo de incubación asintomática con o sin virus detectable.ramonsv@unam.mx
Etapa II. Periodo sintomático no grave con presencia de virus.
3. Etapa III. Etapa sintomática respiratoria grave con alta carga viral.
Los principales síntomas de la enfermedad infecciosa con fiebre de duración prolongada, fatiga, tos seca, dificultad para respirar, dolor muscular y dolor de cabeza. Los síntomas pueden mejorar con una identificación temprana y tratamiento o en caso contrario, empeorar aumentando la disnea y la tos en los pacientes. Después de la exposición hasta el inicio de la disnea en los pacientes tiene una mediana de 6 días. Los pacientes que presentan disnea pueden avanzar a una fase asintomática o desarrollar Síndrome de Déficit Respiratorio Agudo, conocido por sus siglas como SDRA. (Huang, C et al. 2020). La mediana de tiempo desde el ingreso, el desarrollo de SDRA y la necesidad de ventilación mecánica y atención en terapia intensiva se ha reportado de entre 8 y 10 días. (SharmaRetal. 2020).
4. El COVID-19 y su relación con la Enzima Convertidora de Angiotensina II
La Enzima Convertidora de Angiotensina II se ha asociado con la entrada al cuerpo humano por parte del virus. Se ha establecido la existencia dedos Enzimas Convertidoras de Angiotensina (ACE por sus siglas en inglés): la ACE-1 y la ACE-2. La ACE-1 es la responsable de la conversión de angiotensina I en angiotensina II y la ACE- 2 es la que cataliza la conversión de angiotensina II en angiotensina (1-7) y la conversión de angiotensina I y angiotensina II en angiotensina (1,9). (Lorenzo-Velázquez, B. 2015)
La asociación entre SARS-CoV con SARS-CoV-2 se ha estudiado mediante los análisis realizados a la proteína S (espiga) que caracteriza a estos dos virus, donde se dejó en claro una similitud importante en estas estructuras transmembranales. La única porción significativamente distinta es un dominio de unión a furina en la proteína S de SARS-CoV-2, el cual se ha especulado podría expandir el tropismo del virus en el cuerpo humano o incrementar la transmisibilidad del virus en comparación del SARS-CoV de 2003 (Walls, A.C. et al. 2020).
Por otro lado, una de las porciones más conservadas de la proteína S, es el dominio de unión a receptor (RBD por sus siglas en inglés Receptor Binding Domain), el cual presenta una afinidad similar (o según reportes, mayor) a la enzima convertidora de angiotensina tipo 2 (ACE-2) en comparación con SARS-CoV. (Walls, A.C. et al. 2020) (Tai, W, et al. 2020). Este receptor funcional se encuentra en tejidos, incluyendoepitelio alveolar del pulmón, endotelio arterial y venoso, músculo liso, epitelio tubular renal y epitelio del intestino delgado, (Li, M 2020) (The Human Protein Atlas, 2020) explicando en gran medida los síntomas presentes en los pacientes con COVID-19.
Adicionalmente las respuestas inmunes innatas y adaptativas pueden inducir una tormenta de citocinas siendo las responsables del daño inmunopatológico en pacientes con infecciones por COVID-19 (Li G. 2020).
5. Síndrome de Déficit Respiratorio Agudo y la tormenta de citocinas en pacientes con COVID-19
Los exámenes post-mortem realizados a pacientes que fallecieron por COVID-19, muestran que el cuadro clínico de los pacientes culmina con el Síndrome de Déficit Respiratorio Agudo, que es mediado probablemente por la liberación masiva de citocinas.
Se han encontrado altos niveles de varias citocinas proinflamatorias, incluidas IL-6, IL-1, TNF-a, en pacientes en estadio avanzado (Huang, C et al. 2020) (Conti, P et al. 2020) lo que respalda la hipótesis de que el inicio del SDRA es impulsado por pro-citocinas inflamatorias, que son responsables de los cambios histológicos. Entre las citosinas proinflamatorias, la IL-6 parece estar proinflamatorias, incluidas IL-6, IL-1, TNF-a, en muy involucrada, como lo indican los niveles constantemente elevados detectados por PCR.
En la fase exudativa alveolar del SDRA, los macrófagos se activan, lo que lleva a la liberación de mediadores proinflamatorios y quimiocinas que promueven la acumulación de neutrófilos y monocitos. Los neutrófilos activados contribuyen aún más a la lesión mediante la liberación de mediadores tóxicos. La lesión resultante conduce a la pérdida de la función de barrera, así como a la inundación intersticial e intraalveolar. (Thomson, T2017)
En la infección por COVID-19, hay un retraso inicial en la secreción de citocinas y quimiocinas por las células inmunes innatas con el consiguiente aumento de las citocinas y quimiocinas proinflamatorias (IL-6, TNF-a, IL-8, MCP-1, IL-1 p, CCL2, CCL5 e IFN) por los macrófagos activados y otros linfocitos reclutados. Estas citocinas inducen el reclutamiento y la activación de células inmunes adaptativas como las células T, los neutrófilos y las células NK junto con una mayor producción de citocinas proinflamatorias, lo que provoca una tormenta de citocinas y daños en los tejidos. (Lingeswaran, M., et al. 2020).
La IL-6 es una potente citocina proinflamatoria que desempeña un papel principal en la tormenta de citocinas en la infección por el COVID-19. La IL-6 es una citocina multifuncional implicada en la formación de células T auxiliares foliculares, la diferenciación de subconjuntos de células Th17 y la generación de células plasmáticas. También se sabe que inhibe IFN-y y, por lo tanto, suprime las células T citotóxicas CD8 + (Velazquez-Salinas, Netal. 2019)
La IL-ip y su familia (IL-18, IL-33) son citocinas importantes que promueven el SDRA y se sabe que aumentan el reclutamiento de células inmunes y la posterior producción de otras citocinas (Tisoncik JR et al. 2020). La señalización del receptor de IL-1 está implicada en el daño inflamatorio del epitelio respiratorio.
En un estudio, el perfil diario de tres pacientes con la COVID-19 reveló que la IL-1 presenta cambios significativos en la expresión antes del deterioro de la función respiratoria. Todas las otras citocinas proinflamatorias se indujeron solo después de la aparición de síntomas de disfunción respiratoria. Este breve informe insinúa el papel plausible de la vía IL-1 en la progresión inicial de la inmunopatología pulmonar relacionada con COVID-19 (Ong EZ, et al. 2020)
El SDRA inducido por COVID-19 y la mortalidad pueden estar mediados por otros muchos factores. La alteración de los componentes innatos y adaptativos del sistema inmune en términos derespuesta amortiguada de células T, neutrofilia y respuesta retardada de IFN tipo 1 juega un papel importante. Además, el aumento de la expresión de granulisina y perforina, el aumento de las citocinas activadas por macrófagos como IL-1ß, IL-6 y TNF-a que conducen a la tormenta de citocinas y el aumento del agotamiento de las células T podrían contribuir aún más a la patogénesis molecular. Aproximadamente el 15% de los pacientes que padecen COVID-19 progresan a casos graves críticos con síntomas clínicos de insuficiencia respiratoria que requieren asistencia respiratoria. Una tormenta de citocinas acompaña la transición de la forma leve a grave de la enfermedad en pacientes con COVID-19. (Lingeswaran, M., et al. 2020)
6. Protocolos y Estrategias de tratamientos aprobados por Instituciones Internacionales para el tratamiento de COVID-19
La Administración de Alimentos y Medicamentos de los EE. UU. (FDA, por sus siglas en inglés) aprobó el medicamento antiviral Veklury (remdesivir) para su uso en pacientes adultos y pediátricos de 12 años o mayores y que pesen al menos 40 kilogramos (aproximadamente 88 libras) para el tratamiento del COVID-19 que requiera hospitalización.
La aprobación de Veklury fue respaldada por el análisis de datos de la agencia de tres ensayos clínicos controlados aleatorizados que incluyeron pacientes hospitalizados con COVID-19 de leve a grave.
La FDA ha dado autorización de emergencia para la terapia con el plasma de personas convalecientes para tratar pacientes con COVID-19. El plasma de personas convalecientes es sangre donada por personas que se han recuperado de COVID-19. Este plasma se usa para tratar a las personas que están enfermas con COVID-19 e internadas en el hospital.
Dos medicamentos de anticuerpos monoclonales han recibido autorización para uso de emergencia de la FDA. Un medicamento se llama bamlanivimab, y el otro es una combinación de dos anticuerpos, llamados casirivimab e imdevimab. Ambos medicamentos se usan para tratar COVID-19 leve a moderada en personas que están a más alto riesgo de una enfermedad grave a causa de COVID-19.
La FDA autorizó el uso de estos medicamentos contra la malaria en situaciones de emergencia durante la pandemia de COVID-19. Pero la FDA revocó esta autorización cuando el análisis de datos demostró que estos medicamentos no son efectivos en el tratamiento de la COVID-19. También pueden causar graves problemas cardíacos. (Administración de Alimentos y Medicamentos de los EE. UU. FDA, 2020)
La Organización Mundial de la Salud (OMS) anunció un gran ensayo global, llamado SOLIDARIDAD, para probar cuatro principales tratamientos contra las infecciones del nuevo coronavirus (COVID-19).
La OMS se está centrando en lo que dice son las cuatro terapias más prometedoras: un compuesto antiviral experimental llamado remdesivir; los medicamentos contra la malaria llamados cloroquina e hidroxicloroquina; una combinación de dos medicamentos contra el VIH, lopinavir y ritonavir; y esa misma combinación más interferón beta, un mensajero del sistema inmune que puede inhabilitar los virus. (Organización Mundial de la Salud (OMS), 2020)
El remdesivir es el único medicamento que cuenta con autorización de comercialización condicional en la UE para el tratamiento de pacientes con COVID-19 que necesitan suministro de oxígeno.
La transfusión de plasma de convalecientes a pacientes enfermos puede ayudarles a luchar contra la COVID-19. Las transfusiones de plasma también se utilizan para la purificación de anticuerpos, con el fin de elaborar un medicamento específico contra la COVID-19 («inmunoglobulina») como alternativa a corto plazo a las vacunas. Este producto se puede inyectar a los pacientes, las personas vulnerables y los trabajadores sanitarios. La eficacia de ambos enfoques se sigue investigando en todo el mundo, en particular en proyectos de investigación de la UE. (Unión Europea, 2020)
7. La importancia de las patentes en principios activos recomendados para combatir esta pandemia.
En el contexto de una pandemia global, la innovación en la industria farmacéutica es una pieza clave para reducir las cifras de infectados y de muertos, esta industria no solo debe enfocarse en conseguir una vacuna para prevenir la enfermedad, sino generar un tratamiento efectivo y seguro para ello , esto a través de la investigación clínica, valiéndose de muchos métodos de desarrollo y síntesis de nuevas moléculas, asimismo también se vale del descubrimiento de nuevas combinaciones con sinergia terapéutica, todos estos avances deben además ser replicables con seguridad para otros laboratorios, estos criterios de calidad y seguridad son garantizados en gran medida por las patentes,es por esto que juegan un papel tan importante en esta situación. Según la Organización Mundial de la Propiedad Intelectual (WIPO por sus siglas en inglés) una patente es un derecho exclusivo que se concede sobre una invención. En términos generales, una patente faculta a su titular a decidir si la invención puede ser utilizada por terceros y, en ese caso, de qué forma. Como contrapartida de ese derecho, en el documento de patente publicado, el titular de la patente pone a disposición del público la información técnica relativa a la invención.
En principio, el titular de la patente goza del derecho exclusivo a impedir que la invención patentada sea explotada comercialmente por terceros. La protección por patente significa que una invención no se puede producir, usar, distribuir con fines comerciales, ni tampoco vender, sin que medie el consentimiento del titular de la patente.
La protección brindada a la invención desarrollada se concede por un período limitado, que suele ser de 20 años a partir de la fecha de presentación de la solicitud. (Organización Mundial de Propiedad Intelectual, 2020)
En la Industria Farmacéutica, para proteger nuevas moléculas y formulaciones se tienen dos tipos de patentes:Patente de producto. El titular de la patente es el único que tiene la exclusividad de fabricación, ofrecimiento, comercialización, importación y utilización del producto en el país o países en donde la patente ha sido concedida.
Patente de proceso. Es la protección de un procedimiento de obtención de un producto. Este tipo de patente no permite impedir la comercialización, por parte de otra compañía farmacéutica, de un producto original o innovador, obtenido por otro proceso diferente.
Sin embargo; en la práctica encontramos que existen patentes que protegen diferentes aspectos de los productos farmacéuticos, así una clasificación más profunda nos indica diferentes tipos de patentes en el área farmacéutica como son:
1. Patente de molécula, en este caso se protege la invención de una molécula y es la primer patente conocida de un principio activo, a veces se encuentra que una patente de este tipo protege una familia de moléculas al señalar los diferentes sustituyentes en una estructura base, entonces se dice que tenemos una patente tipo Markush, estas patentes pueden incluir además de la molécula la ruta de síntesis y el uso farmacológico.
2. Patente de composición, en este caso se encuentran las patentes que protegen una serie de formulaciones que tienen un común denominador de comportamiento fisicoquímico.
3. Patentes de segundo uso, son las patentes más controversiales, ya que se incluyen a las patentes que describen un segundo uso no conocido y no evidente de una molécula.
4. Patentes de síntesis, son las patentes asociadas a procesos de síntesis de las moléculas farmacéuticas.
5. Patentes de modificación fisicoquímica, cualquier modificación fisicoquímica que se realiza sobre la molécula con objeto de mejorar algún aspecto farmacotécnico de la molécula y que repercute en un mejor manejo, solubilidad, estabilidad o cualquier propiedad fundamental de la molécula.
6. Patentes de polimorfos, los principios activos farmacéuticos sólidos pueden ser amorfos o cristalinos, los cristalinos tienen una estructura de cristalización específica basada en la celda cristalina unitaria y su crecimiento en una forma específica producen diversas estructuras cristalinas específicas que se caracterizan por diferencias sutiles en punto de fusión, solubilidad, estabilidad y sobre todo biodisponibilidad, los polimorfos se caracterizan de manera analítica mediante estudios de Difractometría de Rayos X,Calorimetría de Barrido Diferencial y Microscopía Electrónica, debido a la complejidad de la tecnología asociada en el fenómeno de polimorfismo se encuentra un gran número de patentes en este tema por cada molécula farmacéutica.
7. Patentes de sistemas farmacéuticos, son las patentes que protegen un sistema de liberación, estabilidad fármaco-excipiente, sistema de administración o un sistema eficiente de fabricación de un medicamento, estas patentes incluyen sistemas nanométricos de transporte de fármacos.
Las patentes anteriormente descritas pueden superponerse en el tiempo tal como se muestra en la figura siguiente:

Figura 1. Tipos de Patentes Farmacéuticas y Curva de desarrollo tecnológico S donde se muestra la forma en la cual se superponen las diferentes patentes de un producto farmacéutico, "y" corresponde a el avance dentro del mercado.

Figura 2. Tipos de Patentes Farmacéuticas y Curva de desarrollo tecnológico S donde se muestra la tendencia (curva en color naranja).
8. Estrategias de desarrollo e investigación
Desde el punto de vista estratégico no es conveniente que un investigador farmacéutico invada patentes de cualquier tipo, por el contrario sería deseable que el desarrollo farmacéutico realizado sea capaz de aprobar los exámenes de novedad y de altura inventiva a nivel internacional; por el contrario el investigador deberá conocer profundamente el estado de latécnica (o estado del arte), es decir la investigación que se realice deberá de no ser publicada antes de la solicitud de patente y no haber sido realizada con anterioridad, en el caso de la infección por Covid19, al tratarse de un nuevo virus puede suceder que la aplicación en el tratamiento de esta enfermedad efectivamente no sea conocido; sin embargo, existen otras patentes que el investigador deberá observar, de tal forma que es posible en función a lo anterior señalar en cada una de las moléculas investigadas una semaforización de posibilidades de trabajo con ellas sin la invasión de patentes anteriores.
Metodología
El trabajo se desarrolló en varias etapas. En la primera etapa se recolectó información acerca de la estructura genómica del SARS-CoV-2, los síntomas y diagnóstico, así como las alternativas para el tratamiento de la enfermedad por COVID-19, con el fin de tener un racional farmacológico para las moléculas que poseen actividad importante en el tratamiento de los problemas asociados con la infección por el virus.
En una segunda etapa se realizó un estudio documental de las propiedades químicas, físicas y farmacológicas de cada uno de los principios activos que previa selección con base en su actividad farmacológica se presentan en este trabajo, asimismo se consideró alguna combinación de dos moléculas debido a que la práctica médica así lo ha realizado; los motivos farmacológicos por los cuales se han seleccionado cada uno de los principios activos, para posteriormente presentar un primer acercamiento a la identificación de las patentes de las moléculas de cada principio activo, así como la determinación del año de presentación de cadauna de las mismas con el fin de conocer la vigencia a la fecha de octubre de 2020, entre las bases utilizadas se encuentra chemical index database, https://www.drugfuture.com/chemdata/
En la tercera etapa se realizó una búsqueda en la página del Orange Book de la FDA en la sección de Approved Drug Products with Therapeutic Equivalence Evaluations, acerca de la existencia de productos con estudios de bioequivalencia así como cuántos de estos medicamentos se localizaron y en que forma farmacéutica se encuentran https://www.accessdata.fda.gov/script s/cder/ob/index.cfm
Asimismo, se realizó una búsqueda rápida por nombre del principio activo en la base de datos LATIPAT (base de datos ESPACENET latinoamericana, la cual incluye patentes en español y portugués que desde el año 2003 opera con información de las oficinas nacionales de propiedad intelectual-industrial de Argentina, Bolivia, Brasil, Chile, Colombia, Costa Rica, Cuba, Ecuador, El Salvador, Guatemala, Honduras, México, Nicaragua, Panamá, Paraguay, Perú, República Dominicana, Uruguay y Venezuela bajo el auspicio de Organización Mundial de la Propiedad Intelectual (OMPI), la Oficina Europea de Patentes (OEP) y la Oficina Española de Patentes y Marcas (OEPM) https://lp.espacenet.com/); en algunos casos específicos en los cuales no se localizó información para algún principio activo en las bases de datos anteriores se procedió a realizar una búsqueda por nombre del principio activo en la base de datos de la Oficina Europea de Patentes a nivel mundial, https://worldwide.espacenet.com/patent/search
Para los casos en donde no se localizan patentes de alguno de los principios activos de interés se realizó la búsqueda específica en la Oficina Norteamericana de Patentes y Marcas en la sección de patentes y búsqueda de patentes otorgadas desde 1976, búsqueda rápida http://patft.uspto.gov/netahtml/PTO/search-bool.html. Es importante mencionar que las búsquedas se realizaron entre el 1 y el 15 deCuadro 1. Medicamentos Antiinflamatorios. octubre de 2020.
Es importante mencionar que la búsqueda se realiza previamente con la finalidad de tener una opinión rápida para ser tomada en cuenta en el desarrollo de medicamentos para el tratamiento de COVID-19, sin embargo cuando el proceso de desarrollo se lleva a cabo es necesario realizar una búsqueda profunda de cada una de las moléculas.
Resultados
A continuación, se presentan los resultados, obtenidos después de seguir la metodología descrita, en cada cuadro se encuentran Medicamentos analizados, actividadfarmacológica principal, su estructura, química, propiedades fisicoquímicas y patente de molécula con su vigencia.
Cuadro 1 . Medicamentos Antiinflamatorios








Cuadro 2 . Medicamentos Cardiovasculares







Cuadro 3 . Medicamentos inmunomodulares







Cuadro 4 . Medicamentos Antivirales










Cuadro 5 . Medicamentos inmunosupresores




Cuadro 6 . Medicamentos Antimalaricos
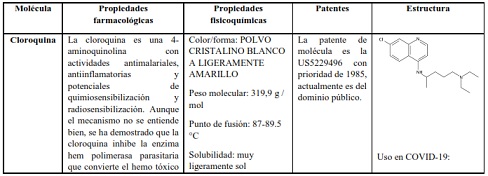






Cuadro 7 . Anticuerpos monoclonales









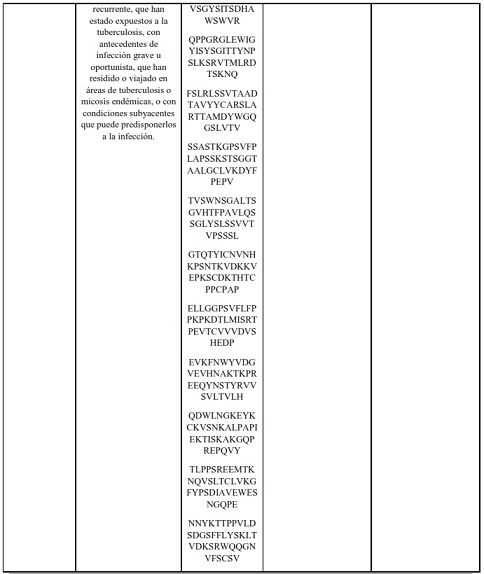





Cuadro 8 . Medicamentos antibioticos


Cuadro 9 . Medicamentos antibioticos


A continuación, se presentan los resultados en relación a las patentes encontradas con base en la posibilidad de desarrollo sin infringir patentes o bien utilizarlas como fuente de información para el trabajo principalmente de medicamentos genéricos se les asigno el código del semáforo, donde se indican a manera de semáforo; verde hay buenas posibilidades, amarillo hay posibilidadesde desarrollo pero se debe ser muy cuidadoso con las patentes relacionadas al principio activo en cuestión, rojo cuando existe alguna patente de molécula, composición o uso que impide el desarrollo de un producto genérico o contra el COVID 19 por lo menos en los próximos 4 años.
Cuadro 10. Estado de las patentes de los principios activos seleccionados por grupo terapéutico.







Fuente: https://www.fda.gov/drugs/biosimilars/biosimilar-product-information
Discusión
La enfermedad por SARS COVID-19 se produce por un virus desconocido hasta ahora, con lo cual se trata de una nueva enfermedad, para la cual no existe cura, esto significa que los principios activos del arsenal farmacéutico actual son parcialmente eficientes para tratar esta enfermedad, los principios activos estudiados permiten el tratamiento de la sintomatología asociada a la infección y ayudan a la recuperación del paciente, pero ninguno de ellos ataca directamente al virus ni evitan la infección, esto mismo desata una importante actividad de investigación sobre todo en el uso de estas moléculas en el tratamiento de esta enfermedad, misma que se considera que puede generar varias patentes de segundo uso o de composición específica.
Una de las primeras observaciones, es que las moléculas de origen químico sintético analizadas en este documento se encuentran en una fase avanzada de la curva S, es decir la tecnología ya está en el techo tecnológico y casi todas las patentes de éstas están vencidas en los diferentes grupos de moléculas con actividad farmacológica antinflamatoria, cardiovascular y antimalárica. Por lo mencionado anteriormente en el caso de los analgésicos y la mayoría de las moléculas estudiadas, su patente ya venció y existe un gran número de medicamentos genéricos. Existe un caso, el piclidenoson cuya patente estará vigente hasta el año 2026, por lo tanto, se reportaron medicamentos genéricos hasta después de esa fecha.
Posiblemente una de las mejores alternativas terapéuticas son los inmunomoduladores, debido a que actúan de manera preventiva, durante la infección y son particularmente útiles, ya que pueden mediar la respuesta agresiva de las citocinas, dentro de este grupo de moléculas se encuentra la molécula Rintatolimod con patente vigente al igual que el Baricitinib.
En el caso de los medicamentos antivirales que son la alternativa que más se explorará por la naturaleza viral de la infección, encontramos que las moléculas con actividad antiviral como el caso del Remdesivir, cuya patente de molécula estará vigente hasta el año 2029 y debido a ello hoy día no existen medicamentos genéricos de este principio activo registrados en Estados Unidos de América.
Por otro lado los medicamentos biotecnológicos, por su mecanismo de acción, son particularmente importantes ya que han presentado actividad contra el COVID-19, sin embargo su fabricación no es fácil y en muchos países aún no existe la tecnología para llevarla a cabo, además la intercambiabilidad, tiene implicaciones importantes, se dice que el proceso de producción tiene un componente esencial en la bioequivalencia del producto final, razones por las cuales no existe prácticamente la bioequivalencia y se denominan biosimilares.
10. Conclusiones
El coronavirus como agente etiológico nuevo, mortal y altamente infeccioso analizando el comportamiento por analogía con la curva "S" podemos observar que tiene su propia tendencia de I & D en el ámbito de la tecnología farmacéutica, médica y epidemiológica. Provocando de forma por demás agresiva la búsqueda de moléculas que tengan actividad contra la enfermedad por COVID-19. Las patentes sin duda nos permiten contribuir a estas tendencias, además de mostrar los derroteros de la investigación y desarrollo tecnológico. Como se puede ver a través de la PI podemos determinar hacia dónde va la tecnología y la solución a problemas y satisfacción de necesidades que permitirán a muchos investigadores de diversos centros, empresas e instituciones por donde buscar. Se pudo apreciar que para contrarrestar al SARS-COV-2, las moléculas que se han estado manejando en los diversos tratamientos tienen patentes cuya vigencia han vencido, ya sea solos o en combinación. La punta de lanza del desarrollo tecnológico en materia de antivirales aún tiene un largo camino hasta que se venzan las patentes y se conozca más de ellos.
Asimismo, los esfuerzos en materia de investigación en vacuna aún hemos visto a través de la PI son profundos cambiando los paradigmas existentes hasta ahora ya que hoy día la ingeniería genética ha provocado el uso de material genético cambiando el concepto a vacunas vectorizadas que transportan cadenas pequeñas de adenovirus por ejemplo, y cuya información está contenida en las patentes, que se han podido encontrar.
Agradecimientos
QFB Yurihelem Jacobo Cruz Consultor en propiedad intelectual farmacéuticaResearch Pro SC
QFB Felix Lugo TrejoConsultor en propiedad intelectual farmacéuticaResearch Pro SC
Referencias
Chan JF-W, Kok K-H, Zhu Z, Chu H, To KK-W, Yuan S, Yuen K-Y (2020) Genomic characterization of the 2019 novel human -pathogenic coronavirus isolated from a patient with atypical pneumonia after visiting Wuhan. Emerg Microb Infect 9:221-236 [ Links ]
Conti P, Ronconi G, Caraffa A, et al. Induction of pro-inflammatory cytokines (IL-1 and IL-6) and lung inflammation by Coronavirus-19 (COVI-19 or SARS-CoV-2): anti-inflammatory strategies [published online ahead of print, 2020 Mar 14]. J Biol Regul Homeost Agents. 2020;34(2):1. doi:10.23812/CONTI-E [ Links ]
Huang C, Wang Y, Li X, et al. Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China [published correction appears in Lancet. 2020 Jan 30;:]. Lancet. 2020;395(10223):497-506. doi:10.1016/S0140-6736(20)30183-5 [ Links ]
Jiang S., Shi Z., Shu Y., Song J., Gao GF, Tan W., Guo D. Se necesita un nombre distinto para el nuevo coronavirus. Lanceta. 2020; 395 : 949. doi: 10.1016 / S0140-6736 (20) 30419-0. [ Links ]
Li, M., Li, L., Zhang, Y. et al. Expresión del gen del receptor de células S ARS-CoV-2 ACE2 en una amplia variedad de tejidos humanos. Infect Dis Poverty 9, 45 (2020). https://doi.org/10.1186/s40249-020-00662-x [ Links ]
Li G, Fan Y, Lai Y, Han T, Li Z, Zhou P, et al. Infecciones por coronavirus y respuestas inmunes. J Med Virol. 2020; https://doi.org/10.1002/jmv.25685 . [ Links ]
Lingeswaran, M., Goyal, T., Ghosh, R. et al. Inflammation, Immunity and Immunogenetics in COVID-19: A Narrative Review. Ind J Clin Biochem (2020). https://doi.org/10.1007/s12291-020-00897-3 [ Links ]
Low-cost dexamethasone reduces death by up to one third in hospitalised patients with severe respiratory complications of COVID-19 [Internet]. [cited 2021 Jan 22]. Available from: https://www.recoverytrial.net/news/low-cost-dexamethasone-reduces-death-by-up-to-one-third-in-hospitalised-patients-with-severe-respiratory-complications-of-covid-19 Clinical Trials.gov [Internet]. [cited 2021 Jan 22]. Available from: https://clinicaltrials.gov/ct2/homeOrange Book: Approved Drug Products with Therapeutic Equivalence Evaluations [Internet], [cited 2021 Jan 22]. Available from: https://www.accessdata.fda.gov/scripts/cder/ob/index.cfmEPO Espacenet: patent database with over 120 million documents [Internet]. [cited 2021 Jan 22]. Available from: https://www.epo.org/searching-for-patents/technical/espacenet.html [ Links ]
Medscape Drugs & Diseases [Internet]. [cited2021 Jan 22]. Avai m lable from: https://reference.medscape.com/ [ Links ]
Ong EZ, Chan YFZ, Leong WY, Lee NMY, Kalimuddin S, Haja Mohideen SM, et al. Una respuesta inmune dinámica da forma a la progresión de COVID-19. Cell Host Microbe.2020 abr; S1931312820301852. [ Links ]
Sharma R., Agarwal M., Gupta M., Somendra S., Saxena SK (2020) Características clínicas y diagnóstico clínico diferencial de la nueva enfermedad por coronavirus 2019 (COVID-19). En: Saxena S. (eds) Enfermedad por coronavirus 2019 (COVID-19). Virología médica: de la patogénesis al control de enfermedades. Springer, Singapur [ Links ]
Shi, Y., Wang, Y., Shao, C. y col. Infección por COVID-19: las perspectivas sobre las respuestas inmunes. Cell Death Differ 27, 1451-1454 (2020). https://doi.org/10.1038/s41418-020-0530-3 [ Links ]
Tai, W., He, L., Zhang, X. et al. Caracterización del dominio de unión al receptor (RBD) del nuevo coronavirus 2019: implicación para el desarrollo de la proteína RBD como inhibidor de la unión viral y vacuna. Cell Mol Immunol 17, 613-620 (2020). https://doi.org/10.1038/s41423-020-0400-4 [ Links ]
Tisoncik JR, Korth MJ, Simmons CP, Farrar J, Martin TR, Katze MG. En el ojo de la tormenta de citoquinas. Microbiol Mol Biol Rev. 2012; 76 (1): 16-32. [ Links ]
Thompson T., Chambers RC, Liu KD, Acute Respiratory Distress Syndrome, [J]. N. ENGL J MED, 2017, 377(6) 562-572.DOI: 10.1056/NEJMra1 608077 [ Links ]
United States Patent and Trademark Office [Internet]. [cited 2021 Jan 22]. Available from: https://www.uspto.gov/ [ Links ]
Velazquez-Salinas L, Verdugo-Rodriguez A, Rodriguez LL, Borca MV. The role of interleukin 6 during viral infections. Front Microbiol. 2019;10(10):1057. [ Links ]
Walls, A. C., Park, Y. J., Tortorici, M. A., Wall, A., McGuire, A. T., & Veesler, D. (2020). Structure, Function, and Antigenicity of the SARS-CoV-2 Spike Glycoprotein. Cell, 181(2), 281-292.e6. https://doi.org/10.1016/j.cell.2020.02.058 [ Links ]
Xu X, Chen P, Wang J et al (2020) Evolución del nuevo coronavirus a partir del brote en curso de Wuhan y el modelado de su proteína espiga para el riesgo de transmisión humana [J]. Sci China Life Sci 63 (3): 457-60 [ Links ]
Yoshimoto, F.K. The Proteins of Severe Acute Respiratory Syndrome Coronavirus-2 (SARS CoV-2 or n-COV19), the Cause of COVID-19. Protein J 39, 198-216 (2020). https://doi.org/10.1007/s10930-020-09901-4 [ Links ]














