Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de la Sociedad Boliviana de Pediatría
versión On-line ISSN 1024-0675
Rev. bol. ped. v.44 n.1 La Paz ene. 2005
ACTUALIZACION
Neonatal hyperbilirubinemia
Ac. Dr. Eduardo Mazzi Gonzales de Prada*
| * | Profesor de Pediatría. Facultad de Medicina. UMSA Jefe. Servicio de Hospitalización Médica. Hospital del Niño “Ovidio Aliaga Uría “. La Paz Teléfonos: 24030350-2246151, correo electrónico: doctormazzi@yahoo.com Dirección: Casilla de correo 4076. La Paz |
Introducción
Desde las últimas recomendaciones emitidas por la Academia Americana de Pediatría hace diez años, se publican en octubre del año 2004 nuevas recomendaciones para el manejo de la hiperbilirrubinemia neonatal y la prevención de sus secuelas neurológicas. La hiperbilirrubinemia neonatal se manifiesta como la coloración amarillenta de la piel y mucosas que refleja un desequilibrio temporal entre la producción y la eliminación de bilirrubina. Las causas de ictericia neonatal son múltiples y producen hiperbilirrubinemia directa, indirecta o combinada, de severidad variable.
Aproximadamente el 50-60% de neonatos presentan hiperbilirrubinemia y la mayoría de los recién nacidos desarrollan ictericia clínica luego del segundo día de vida como expresión de una condición fisiológica. La ictericia en la mayoría de los casos es benigna, pero por su potencial neurotoxicidad, debe ser monitorizada muy de cerca para identificar neonatos que pueden desarrollar hiperbilirrubinemia severa y alteraciones neurológicas inducidas por la bilirrubina.
Esta actualización tiene como objetivo revisar el tema y actualizar las nuevas recomendaciones y publicaciones al respecto, para lo cual, se revisaron artículos relevantes publicados en los últimos cinco años en revistas científicas y buscando en Internet trabajos científicos sobre hiperbilirrubinemia neonatal, encefalopatía bilirrubínica y kernicterus.
Fisiopatología
El recién nacido en general tiene una predisposición a la producción excesiva de bilirrubina debido a que posee un número mayor de glóbulos rojos cuyo tiempo de vida promedio es menor que en otras edades y muchos de ellos ya están envejecidos y en proceso de destrucción; además que el sistema enzimático del hígado es insuficiente para la captación y conjugación adecuadas. La ingesta oral está disminuida los primeros días, existe una disminución de la flora y de la motilidad intestinal con el consecuente incremento de la circulación entero-hepática. Finalmente, al nacimiento el neonato está expuesto a diferentes traumas que resultan en hematomas o sangrados que aumentan la formación de bilirrubina y además ya no existe la dependencia fetal de la placenta. Cuadro # 1.
La mayoría de la bilirrubina deriva de la hemoglobina liberada por la destrucción del eritrocito. El factor hem por la acción de la enzima hemo-oxigenasa se transforma en biliverdina, produciéndose además monóxido de carbono que se elimina por los pulmones y hierro libre que puede ser reutilizado en la síntesis de hemoglobina. La biliverdina se convierte en bilirrubina por acción posterior de la biliverdina reductasa (NADPH). Esta bilirrubina se denomina indirecta o no conjugada y es un anión liposoluble y tóxico en su estado libre. Un gramo de hemoglobina produce 35 mg de bilirrubina y aproximadamente se forman 8-10 mg de bilirrubina al día por cada kilogramo de peso corporal.
La albúmina capta dos moléculas de bilirrubina indirecta. La primera se une fuertemente a la bilirrubina, pero la segunda tiene una unión lábil y puede liberarse fácilmente en presencia de factores clínicos (deshidratación, hipoxemia, acidosis), agentes terapéuticos (ácidos grasos por alimentación parenteral) y algunas drogas (estreptomicina, cloranfenicol, alcohol benzílico, sulfisoxasole, ibuprofeno), que compiten con esta unión y liberan bilirrubina en forma libre a la circulación. Un gramo de albúmina puede unir hasta 8, 2 mg de bilirrubina. La bilirrubina indirecta libre penetra fácilmente al tejido nervioso causando encefalopatía bilirrubínica.
Al llegar la bilirrubina al hepatocito se desprende de la albúmina y es captada en sitios específicos por las proteínas Y-Z (ligandinas), cuyos niveles son bajos los primeros 3-5 días de vida, las cuales transportan la bilirrubina indirecta al interior del hepatocito hacia el retículo endoplásmico liso, donde se lleva a cabo la conjugación, siendo la enzima más importante la uridil difosfoglucuronil transferasa-UDPGT y el producto final un compuesto hidrosoluble, la bilirrubina directa o glucuronato de bilirrubina.
La bilirrubina directa o conjugada es excretada activamente hacia los canalículos biliares, la vesícula biliar y luego al intestino, donde la acción de las bacterias la transforman en urobilinogeno. La ausencia o escasa flora bacteriana, el inadecuado transito intestinal y la enzima beta glucuronidasa produce desconjugación de la bilirrubina que es reabsorbida por el intestino, incrementando la circulación entero hepática. Figura # 1.
Presentación Clínica
La bilirrubina es visible con niveles séricos superiores a 4-5 mg/dL. Es necesario evaluar la ictericia neonatal con el niño completamente desnudo y en un ambiente bien iluminado, es difícil reconocerla en neonatos de piel oscura, por lo que se recomienda presionar la superficie cutánea.
Con relación a los niveles de bilirrubina y su interpretación visual errada, es común que se aprecie menor ictericia clínica en casos de piel oscura, policitemia, ictericia precoz y neonatos sometidos a fototerapia y que se aprecie más en casos de ictericia tardía, anemia, piel clara, ambiente poco iluminado y prematuros.
La ictericia neonatal progresa en sentido céfalo-caudal y se puede estimar en forma aproximada y práctica aunque no siempre exacta, los niveles de séricos de bilirrubina según las zonas corporales comprometidas siguiendo la escala de Kramer. Figura # 2.
Existen dos patrones clínicos de presentación de la ictericia neonatal, sin considerar la etiología y como base para el manejo:
| 1. | Hiperbilirrubinemia severa temprana, generalmente asociada a una producción incrementada por problemas hemolíticos y presente antes de las 72 horas de vida. |
| 2. | Hiperbilirrubinemia severa tardía, generalmente asociada a una eliminación disminuida, que puede o no asociarse a incremento de su producción y presente luego de las 72 horas de vida. Generalmente se debe a problemas de lactancia o leche materna, estreñimiento, mayor circulación entero hepática, etc. El cribado de bilirrubina al alta la reconoce y de acuerdo a sus percentilos en el nomograma horario se instituye el manejo correspondiente. |
Ictericia patológica
A diferencia de la ictericia transitoria fisiológica, la patológica necesita una evaluación y seguimiento para tomar las medidas necesarias y evitar su incremento y probable neurotoxicidad. Se acepta como hiperbilirrubinemia patológica, cuando se comprueban los siguientes parámetros. Cuadro # 2.
Complicaciones
La encefalopatía bilirrubínica o toxicidad aguda y el kernicterus o toxicidad crónica se usan actualmente en forma intercambiable y se deben a la deposición de bilirrubina no conjugada en el cerebro. Cuando la cantidad de bilirrubina libre no conjugada sobrepasa la capacidad de unión de la albúmina, cruza la barrera hematoencefálica y cuando ésta, está dañada, complejos de bilirrubina unida a la albúmina también pasan libremente al cerebro. La concentración exacta de bilirrubina asociada con la encefalopatía bilirrubínica en el neonato a término saludable es impredecible.
A cualquier edad, cualquier neonato ictérico con cualquier signo neurológico sospechoso de encefalopatía bilirrubínica debe asumirse que tiene hiperbilirrubinemia severa o al contrario, cualquier recién nacido con hiperbilirrubinemia severa debe considerarse sospechoso de encefalopatía bilirrubínica hasta que se demuestre lo contrario.
Existe una reemergencia de kernicterus en países donde virtualmente había desaparecido, fenómeno debido principalmente al alta temprana de los neonatos sin asegurar seguimiento apropiado ni dar información adecuada a los padres. Cuadro # 3
Varios investigadores atribuyen la re emergencia del kernicterus , a diferentes factores que se mencionan en el cuadro # 4.
La sintomatología de la neurotoxicidad de la bilirrubina es compleja, se resumen las manifestaciones clínicas más importantes en el cuadro # 5.
Exámenes complementarios
En general son pocos los exámenes requeridos en la mayoría de los casos y se necesita solamente determinar el grupo y Rh sanguíneo materno y del neonato, bilirrubina sérica, hematocrito o hemoglobina, recuento de reticulocitos, prueba de Coombs y frotis sanguíneo.
De acuerdo a la situación clínica, se puede evaluar la hiperbilirrubinemia de acuerdo a las sugerencias descritas en el cuadro # 6.
Causas de hiperbilirrubinemia neonatal
La hiperbilirrubinemia neonatal se debe a múltiples causas y se la puede clasificar en tres grupos de acuerdo al mecanismo causante: producción incrementada, disminución de la captación y conjugación y disminución o dificultad en su eliminación. Cuadro # 7.
Ictericia secundaria a la leche materna
Ictericia infrecuente y más tardía, sin una patogenia definida, se culpa a la existencia de ácidos grasas o beta glucoronidasa en la leche que inhiben el metabolismo normal de la bilirrubina. La bilirrubinemia disminuye gradualmente y puede persistir por tres a diez semanas.
Ictericia secundaria a mala técnica de lactancia materna
Ictericia más frecuente y temprana por mala técnica de lactancia, deprivación calórica, frecuencia y volumen de alimentación disminuidos, ayuno prolongado, que resultan en estreñimiento y deshidratación. Además de escasa flora intestinal y mayor actividad de beta glucuronidasa que incrementan la circulación enterohepática. Se debe implementar habitación compartida, lactancia frecuente y a demanda, evitando la ingesta de otros líquidos para disminuir su presentación.
Ictericia persistente
Es aquella hiperbilirrubinemia que persiste por más de dos semanas. La elevación de la bilirrubina indirecta generalmente sugiere hemolisis, galactosemia, ictericia secundaria la leche materna, hipotiroidismo, obstrucción intestinal, como causas más frecuentes.
Hiperbilirrubinemia conjugada
La hiperbilirrubinemia directa ≥ 2 mg/dL o mayor al 20% de la bilirrubina sérica total, en cualquier momento de la vida, se considera patológica y necesita una evaluación completa. Las características clínicas sobresalientes son la ictericia, hipo/acolia y coluria. Generalmente se necesita recurrir a múltiples exámenes complementarios para su confirmación o exclusión. El tratamiento depende de la causa y será sencillo en ciertos casos y complicado en otros, recurriéndose incluso a la cirugía y trasplante de hígado.
Manejo
El manejo correcto de la hiperbilirrubinemia se basa en el reconocimiento de factores de riesgo y/o en los niveles de bilirrubina sérica total específica para la edad post natal del neonato.
Factores de riesgo. El desarrollo de hiperbilirrubinemia severa depende de factores de riesgo mayores y menores que se deben investigar en todo recién nacido, puesto que la presencia de éstos alerta al médico a la probabilidad de que el neonato desarrolle ictericia severa. Mencionamos los más importantes. Cuadro # 8.
Es la determinación del nivel de bilirrubina y su relación con la edad en horas del recién nacido saludable, con una edad gestacional mayor a las 35 semanas y peso superior a los 2000 g, sin evidencia de hemólisis u otra enfermedad grave. El nomograma permite predecir la severidad de la hiperbilirrubinemia con bastante precisión. Consta de tres zonas: de alto riesgo, de riesgo intermedio y de bajo riesgo y de acuerdo a estas zonas se guía el manejo.
La meta principal del nomograma es la de ayudar en forma rápida, exacta y sencilla, identificar aquellos que desarrollaran hiperbilirrubinemia severa y tomar las previsiones respectivas. Algunos autores la consideran como la manera más exacta de evaluar la hiperbilirrubinemia neonatal, inclusive recomiendan determinarla en forma rutinaria en todos los recién nacidos antes del alta, sobre todo aquellos que son externados antes de la 24 horas de vida. Cuadro # 9.
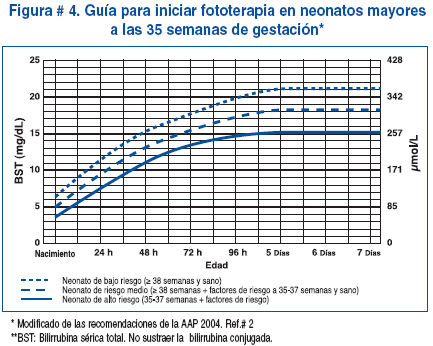
Prevención de la hiperbilirrubinemia severa
La Academia Americana de Pediatría el año 2004, publica recomendaciones para evitar la hiperbilirrubinemia severa y sus consecuencias neurotóxicas y disminuir un daño no intencionado. Estas recomendaciones las enunciamos en cuadro # 10
Tratamiento de la Hiperbilirrubinemia neo-natal
El objetivo principal y de mayor importancia en el tratamiento de la ictericia neonatal es evitar la neurotoxicidad, la disfunción neurológica aguda que induce y su consecuencia neurológica tardía, el kernicterus. El recién nacido pretérmino es el más susceptible, pero cada vez hay más informe de kernicterus en recién nacidos a término o casi término. Todavía existe confusión acerca de los niveles de bilirrubina que producen el daño neurológico.
Los siguientes niveles de bilirrubina sérica total (BST) deben tenerse en cuenta y aplicar el manejo respectivo, además de conocer su incidencia. Cuadro # 11.
Actualmente se sugiere encarar en forma más racional y dinámica el manejo de la ictericia neonatal, evaluando el equilibrio de la producción / eliminación, mediante la determinación del CO en el aire espirado (producción) y la evaluación del nomograma horario de bilirrubina (eliminación), éste último, parámetro es el más utilizado y efectivo y no así el primero. Cuadro # 12.
Debido al alta hospitalaria temprana, es necesario un seguimiento universal y cercano de todos los bebés. Algunos autores recomiendan encarar el problema de forma protocolizada, utilizando el cribado de bilirrubina antes del alta, la velocidad de incremento de la bilirrubina, el tratamiento efectivo para disminuir el exceso de bilirrubina y la evaluación y documentación de signos sugestivos de encefalopatía inducida por la bilirrubina. Este manejo se basa en la evaluación de los niveles y percentilos de la bilirrubina antes del alta y ayudan a estimar el desarrollo de hiperbilirrubinemia severa. Cuadros # 13 y # 14.
Como principio general es importante mantener una hidratación adecuada, ya sea incrementando y estimulando la alimentación oral y/o canalizando una vena que permita la administración de fluidos. Los principales tratamientos comprenden a la luminoterapia, tratamiento farmacológico y el recambio sanguíneo.
Luminoterapia
Desde 1958 se viene utilizando la luminoterapia o fototerapia convencional e intensiva, utilizando la luz blanca o la azul fluorescentes con excelentes resultados. Su efecto es local, actuando sobre la bilirrubina circulante a través de los capilares cutáneos, transformándola en isómeros no tóxicos (lumirrubina) e hidrosolubles.
Existe una relación directa entre la intensidad de la luz, la superficie expuesta de la piel y su efecto terapéutico. Es importante cambiar de posición al paciente y tener la mayor superficie corporal desnuda expuesta a los efectos de la luminoterapia, con excepción de los ojos que deben estar cubiertos, para evitar posibles daños retinianos.
La luminoterapia se utiliza en forma continua, aunque la forma intermitente es también efectiva. De esta manera no limitamos el tiempo de contacto del niño con su madre y mantenemos la lactancia materna exclusiva a libre demanda. La dosis lumínica útil está entre 6-9 mw/cm2/ nm, en la longitud de onda entre 420-500 nm.
Generalmente se utiliza la luz blanca o la luz azul con un mínimo de seis de tubos. La distancia pacienteluminoterapia aconsejada es de 20-30 cm, con una protección plástica (plexiglas) para evitar la irradiación infrarroja y los accidentes casuales. La vida media de los tubos de luz es de aproximadamente 2000 h u 80 días de uso continuo Se recomienda verificar con cada productor de tubos, su tiempo de vida útil y no caer en la”focoterapia” o luminoterapia inefectiva por el uso de tubos viejos sin actividad terapéutica.
La luminoterapia es el método mayormente utilizado para el tratamiento y profilaxis de la ictericia neonatal indirecta. Disminuye los niveles de bilirrubinemia independientemente de la madurez del neonato, la presencia o no de hemólisis o el grado de ictericia cutánea y disminuye la necesidad de recambio sanguíneo. La efectividad de la luminoterapia guarda una relación directa con los niveles de bilirrubina sérica, a mayores niveles mayor efectividad. Figura # 3
Se recomienda suspender la luminoterapia cuando se comprueba descenso de los niveles de bilirrubina en 4-5 mg/dL y por debajo de 14-15mg/dL. El efecto de rebote es menor a un mg/dL y es infrecuente.
Se describen como efectos adversos inmediatos el incremento en el número de las deposiciones, eritemas, distensión abdominal y deshidratación, situaciones que mejoran al descontinuar el tratamiento. Se ha descrito el síndrome del bebé bronceado por la coloración que adquiere la piel del niño expuesto a luminoterapia con niveles elevados de bilirrubina directa. Figura # 4.
Tratamiento farmacológico
El fenobarbital es un potente inductor enzimático, especialmente de la glucuronil-transferasa mejorando la conjugación de la bilirrubina. Se aconseja administrar entre 2-5 mg/kg/día en tres dosis por 7-10 días. Su acción es tardía y se necesita 3-4 días para obtener niveles séricos terapéuticos. El tratamiento exclusivo con fenobarbital o asociado con luminoterapia adecuada, utilizado en forma cautelosa y en circunstancias especiales, puede evitar el recambio sanguíneo.
El agar gel o carbón administrados por vía oral, son sustancias no absorbibles que se unen a la bilirrubina intestinal, facilitando su eliminación, disminuyendo el círculo entero-hepático.
Las protoporfirinas como la protoporfirina-estaño (PPSn) y la mesoporfirina estaño (MPSn), han sido utilizadas recientemente en casos de hiperbilirrubinemia de diversas causas con resultados favorables. Estos compuestos se fijan a la hemo-oxigenasa más ávidamente que el propio factor hem, bloqueando de esta manera el acceso del sustrato natural al punto de fijación de la enzima inhibiendo la degradación del factor hem y por consiguiente la producción de bilirrubina. Como estos compuestos no contienen hierro y por lo tanto no pueden fijar el oxígeno, no pueden ser transformados oxidativamente en bilirrubina por la enzima hemooxigenasa, por lo que permanecen intactos hasta que se excretan. Los compuestos se presentan en viales para inyección intramuscular (20 umol/mL); la dosis recomendada es de 6 umol/kg IM en dosis única en las primeras 24 horas después del nacimiento.
La gammaglobulina intravenosa se recomienda para disminuir la hemólisis, sobre todo en casos de incompatibilidad de grupo en dosis de 0,5-1 g por kg administrada en dos horas, pudiendo repetirse si es necesario.
Recambio sanguíneo
Este procedimiento se reserva para los casos refractarios a las medidas anteriores y para los de hemólisis severas, es muy efectivo para la remoción de anticuerpos antieritrocitarios y bilirrubina, así como para reponer hemoglobina, disminuir la anemia y mejorar el volumen plasmático. Mientras se prepara el recambio sanguíneo, se debe colocar al neonato bajo luminoterapia intensiva y realizar controles seriados de bilirrubina sérica total.
La tendencia actual es tratar de evitarla, puesto que es un procedimiento cruento que necesita espacio e instrumental estéril, costoso en tiempo y dinero y la utilización de sangre implica el riesgo de transmisión de múltiples enfermedades.
En casos de prematuros, se sugiere evitar que el nivel de bilirrubina indirecta sobrepase el equivalente al 1% del peso del neonato, hasta los 2000 g de peso.
Las indicaciones para realizar el recambio sanguíneo se mencionan en la figura # 5.
Ictericia del prematuro
La ictericia visible es casi universal en todos los recién nacidos prematuros y la ictericia fisiológica persiste por más de una semana sin tratamiento con niveles de bilirrubina total dentro de rangos fisiológicos. La fototerapia profiláctica al nacimiento o al momento de diagnosticarla, no es sustentada por la mayoría de los investigadores. A continuación vemos la sugerencia del manejo de la ictericia neonatal del prematuro y de acuerdo al peso de nacimiento en niños con peso inferior a los 2500 g. Cuadro # 14.
Resumimos los mecanismos de acción de las diferentes modalidades de terapia utilizadas en el tratamiento del ictericia neonatal. Cuadro # 15
A continuación se muestra la relación entre los factores involucrados en la producción y eliminación de la bilirrubina y los niveles donde actúan diferentes tratamientos. Figura # 6
Tratamiento urgente de la hiperbilirrubinemia severa
Una vez reconocido cualquier signo de encefalopatía bilirrubínica o si los niveles de la bilirrubina sérica total sobrepasan >30 mg/dL o si la luminoterapía intensiva no disminuye los niveles de bilirrubina < 0.5 mg/dL/h, la meta del tratamiento es la pronta, rápida y segura reducción de la sobrecarga de bilirrubina. Para lo cual se sugiere recambio sanguíneo como único método efectivo para eliminar bilirrubina en un neonato sintomático y disminuir el daño cerebral, utilizando mientras uno se alista, luminoterapia intensiva (>30 µW/cm2/nm con el propósito de reducir los niveles de bilirrubina > 0.5 mg/dL/h.


A continuación resumimos el manejo de la hiperbilirrubinemia neonatal, sugerido por Bhután y colaboradores. Figura # 6.
Finalmente mencionamos el algoritmo sugerido para el manejo de la hiperbilirrubinemia neonatal, desarrollado y utilizado en el Hospital de Niños de Pennsylvania. Figura # 7
Concluimos mencionando que la ictericia neonatal debe ser considerada de suma importancia y ser valorada en forma rutinaria, conjuntamente con los signos vitales en la evaluación diaria del recién nacido y considerar los factores de riesgo que nos orientan a la probabilidad de desarrollar hiperbilirrubinemia severa. Determinar la bilirrubina sérica total relacionándola con el nomograma horario, para que finalmente con estos datos, determinar la conducta y tratamiento correctos y evitar la morbilidad y mortalidad asociada a esta patología.
Referencias
1. American Academy of Pediatrics. Provisional Committee for quality improvement and subcommittee on hyperbilirubinemia. Pediatrics 1994; 94: 558-62. [ Links ]
2. American Academy of Pediatrics. Clinical Practice Guideline. Subcommittee on hyperbilirubinemia. Management of hyperbilirubinemia in the newborn infant 35 or re weeks of gestation. Pediatrics 2004; 114:297–316.
3. Agarwal R, Kaushal M, Aggarwal R, Deorari PK. Early neonatal hyperbilirubinemia using first day serum bilirubin level. Indian Pediatrics 2002; 39: 724-30. [ Links ]
4. Bhutani VK, Donn SM, Johnson LH. Risk management of Severe Neonatal Hiperbilirubinemia to Prevent Kernicterus. Clin Perinatol 2005; 32:125-139 [ Links ]
5. Dennery PA, Seidman DS, Stevenson DK. Drug therapy:neonatal hiperbilirubinemia. N Engl J Med 2001; 344:581-90. [ Links ]
6. Dennery PA. Metallophorphyrins for the treatment of neonatal jaundice. Curr Opin Pediatr 2005; 17: 167-9. [ Links ]
7. Hansen TW. Mechanisms of bilirubin toxicity: clinical implications. Clin Perinatol 2002; 29: 765-78. [ Links ]
8. Kaplan M, Muraca M, Hammerman C, Rubaltelli F, Vilei M, Vreman H, Stevenson D. Imbalance between production and conjugation of bilirubin: a fundamental concept in the mechanism of neonatal jaundice. Pediatrics 2002; 110: e47. [ Links ]
9. Keren R, Bhutani VK, LuanX, Nihyianova S, Cnaan A, Schwartz JS. Identifying newborns at risk of significant hypwerbilirubinaemia: a comparison of two recommended approaches. Arch Dis Child 2005; 90: 415-21. [ Links ]
10. Kobeng AK. Clinical evidence concise. Neonatal jaundice. Am Fam Phisician 2005;71(5):947-64. [ Links ]
11. Kramer LI. Advancement of dermal icterus in the jaundice newborn. Amer J Dis Child 1969; 118: 454-8. [ Links ]
12. Martinez JC. Ictericia neonatal: existe un nivel seguro de bilirrubina?. Arch Argent Pediatr 2002; 100: 321-5. [ Links ]
13. Mazzi E. Ictericia neonatal. En: Mazzi E, Sandoval O, eds. Perinatología. 2da ed. La Paz: Elite Impresiones; 2002.p.483-501. [ Links ]
14. Mazzi E. Ictericia neonatal. En: Díaz M, Tamayo L, Aranda E, Sandoval O, Mazzi E, Bartos A, Peñaranda RM, Quiroga C, eds. Texto de la Cátedra de Pediatría. 2da.ed. La Paz: Elite Impresiones; 2004.p.140-6. [ Links ]
15. Newman TB, Liljestrand P, Escobar GJ. Combining clinical risk factors with serum bilirubin levels to predict hyperbilirubinemia in newborns. Arch Pediatr Adolesc Med 2005; 159:113-9. [ Links ]
16. Porter ML, Dennos BL. Hyperbilirubinemia in the term newborn. Am Fam Physician 2002; 65: 599-606. [ Links ]
17. Ratnavela N, KevinIves N. Investigation of prolonged neonatal jaundice. Curr Paediatr 2005; 15: 85-91. [ Links ]
18. Sarin SU, Serdan MA, Korkmas A, Erden G, Oran O, Tekinalp G et al. Incidence, course, and prediction of hiperbilirubinemia in near-term and term newborns. Pediatrics 2004; 113: 775-80. [ Links ]
19. Sarici SU, Muhittin AS, Korkmaz A. Incidence, course, and prediction of hyperbilirubinemia in near-term and term newborns. Pediatrics 2004;113: 775-80. [ Links ]
20. Schwoebel A, Bhutani VK, Johnston L.Kernicterus: A “never-event” in healthy term and near-term newborns. NBIN 2004; 4 (4): 201-10.
21. Stevenson DK, Wong RJ, Vrema HJ. NICHD conference on kernicterus: research on prevention of bilirubin-induced brain injury and kernicterus: bench-to-bedside: diagnostic methods and prevention and treatment strategies. J Perinatol 2004; 24:521-5. [ Links ]
22. Slusher TM, Angyo IA, Bode-Thomas F, et al. Transcutaneous bilirubin measurements and serum total bilirubin levels in indigenous African infants. Pediatrics 2004; 113:1636-41. [ Links ]
23. Shapiro SM. Definition of the clinical spectrum of kernicterus and bilirubin-induced neurologic dysfunction (BIND).J Perinatol 2005; 25: 54-9. [ Links ]
24. Totapally BR, Torbati D. Neonatal jaundice. Int Pediatr 2005; 20: 47-54. [ Links ]
25. Vinod K, Bhután MD, Lois H, Jonson MD, Karen R. Diagnosis and management of hyperbilirubinemia in the term neonate: for a safer first week. Pediatr Clin North Am 2004; 51: 1-24 [ Links ]