Cuadernos Hospital de Clínicas
versión impresa ISSN 1562-6776
Cuad. - Hosp. Clín. v.61 n.2 La Paz dic. 2020
CASOS CLÍNICOS
Tumor retroperitoneal (Presentación de un Caso Clínico)
Retroperitoneal tumor (Presentation of a Clinical Case)
Campohermoso-Rodríguez O F1, Sardan-D. G2, Soliz-Soliz. R E3, Campohermoso-Rodríguez O4, Villalobos-Q. J5
1. Médico Cirujano, Docente Emérito de Medicina, UMSA. Ginecólogo Obstetra
2. Médico Cirujano, Ginecólogo Obstetra, Hospital Metodista.
3. Médico Cirujano, UMSA. Salud Reproductiva y Sexual.
4. Médico Cirujano, UMSA. Docente de Anatomía Humana, UMSA y UNIVALLE.
5. Licenciado en Enfermería, Instrumentador Quirúrgico
Autor para correspondencia: Ornar Félix Campohermoso Rodríguez, Facultad de Medicina, Universidad mayor de San Andrés, Av. Saavedra 2246, La Paz - Bolivia, campohermoso0701@yahoo.es
INTRODUCCIÓN
Los tumores retroperitoneales son patologías poco frecuente, que se origina del mesodermo embrionario y están usualmente localizadas en músculo, grasa y tejido conectivo.1 Los tumores retroperitoneales primarios son aquellos tumores sólidos o quísticos, benignos o malignos, que se desarrollan en el espacio retroperitoneal a partir de tejidos (linfático, nervioso, vascular, muscular de sostén, conectivo, adiposo y fibroareolar) independientes de los órganos y los grandes vasos (cava inferior y aorta abdominal) contenidos en él como el riñon, las glándulas suprarrenales y las partes retroperitoneales del páncreas, colon y duodeno.2
Se incluyen también los tumores formados a partir de remanentes embriológicos de la cresta urogenital (conductos wolffianos, müllerianos y células germinales) y de la notocorda primitiva.3 También se consideran tumores retroperitoneales primarios los derivados de la cresta neural como los paragangliomas del órgano de Zuckerkandl o de otras localizaciones y los neuroblastomas de localización retroperitoneal extraadrenal.4
El espacio retroperitoneal es una cavidad virtual situada en la parte posterior de la cavidad abdominal, entre el peritoneo parietal posterior y la fascia transversalis y la fascia toracoabdominal que cubre a los músculos de la región lumbar. El plano posterior se inicia desde la duodécima costilla en la parte superior, por la cresta ilíaca, fosa iliaca y el sacro en la porción inferior, extendiéndose desde la cara inferior del diafragma, por arriba, hasta el suelo de la pelvis por debajo, llegando lateralmente hasta el borde externo de los músculos lumbares. Por delante, el espacio retroperitoneal está cerrado por la hoja posterior del peritoneo a través del cual toma contacto con la superficie posterior del hígado, una porción del duodeno-páncreas y parte del colon ascendente y descendente.56
El primer informe de un tumor retroperitoneal fue realizado por Giovanni Battista Morgagni (1682-1771), quien describió en 1761 un tumor lipomatoso en la autopsia de una mujer de 60 años de edad;7 pero fue Jean Fréderic Lobstein (1777-1835) de Estrasburgo quien acuñó el término "tumor retroperitoneal" en su Traite d'anatomiepathologique en 1829.89
Los tumores retroperitoneales representan de 0.3 a 0.8% de todas las neoplasias.10 Cerca del 10 al 15% de los sarcomas tiene un origen retroperitoneal, en los Estados Unidos la incidencia anual calculada es de alrededor de 2,6 casos porcada 1.000.000 de habitantes.11 Aunque parece que la incidencia entre poblaciones a nivel mundial no difiere de la anteriormente anotada, ni hay variaciones por género, hay pocas series a este respecto en Latinoamérica y en nuestro país.
La clasificación de los tumores retroperitoneales primarios no ha variado excesivamente desde la tradicional clasificación de Ackerman en 1954.12

La Clínica es variada en síntomas y signos:13
• Crecimiento asintomático del tumor, con diagnóstico tardío y gran tamaño del tumor.
Síndrome paraneoplásico: Náuseas, vómitos. Anorexia y pérdida de peso. HTA.
Masa abdominal, palpable en etapas tardías (80%). Masa palpable generalmente en la línea media, extendiéndose de forma variable hasta la pelvis y regiones lumbares.
• Síntomas compresivos derivados del crecimiento de la masa: Dolor abdominal, estreñimiento. Hematemesis, hemorroides, hematoquecia. Lumbalgia y ciatalgia. Cólico nefrítico (atrapamiento ureteral en el 60-75%). Retención aguda de orina, disuria, polaquiuria y hematuria.
El diagnóstico clínico es por lo siguiente:14
• Masa palpable generalmente en la línea media, extendiéndose de forma variable hasta la pelvis y regiones lumbares.
• La consistencia de los tumores puede orientar hacia el tipo de lesión, de forma general se describen que las lesiones benignas suelen ser blandas mientras que las duras suelen ser malignas.
Aumento del índice de masa corporal.
• Presencia de circulación colateral abdominal. Edemas en miembros inferiores.
Ecografía, Resonancia magnética o Tomografía
La Ecografía es el primer método por imágenes empleado en el diagnóstico de patología pélvica. Permite conocer las dimensiones del tumor, su localización y textura. Puede identificar metástasis hepáticas y compresiones de los grandes troncos venosos. Sin embargo, la frecuente interposición de gas en los tumores inframesocoiónicos limita la utilidad del método. La tomografía computada es ideal para evaluar retroperitoneo. Los músculos como los cuerpos vertebrales, vasos y ganglios pueden ser identificados. Los diferentes coeficientes de absorción permiten presumir la histología, esto es especialmente válido para el liposarcoma.
La resonancia nuclear magnética ofrece imágenes de gran nitidez. Su mayor ventaja es la excelente definición de los grandes vasos. El diagnóstico preoperatorio del tipo anatomopatológico del tumor puede obtenerse mediante citología o biopsia guiada por ecografía o tomografía computada. La citología con aguja de Chiba puede no ser suficiente para definir la histología. En estos casos, la biopsia con agujas de tipo tru-cut permite obtención de muestra suficiente.
La cirugía es el pilar del tratamiento y la única terapia curativa, debido especialmente a que los tratamientos sistémicos no suelen ser efectivos y la aplicación de la radiación es limitada en esta zona anatómica. El control local de la enfermedad depende de radicalidad de la cirugía, comprometiendo no solo la recurrencia local sino la supervivencia. Suele ser un reto en el manejo debido a que porsu localización alcanzan grandes tamaños, con sintomatología tardía e invasión a estructuras contiguas, lo cual dificulta el logro de márgenes negativos de resección y ocasiona frecuentes resecciones multiviscerales.15
CASO CLÍNICO
Mujer de 45 años, soltera, con cuadro clínico de evolución de un año, que presenta sangrado vaginal moderado, intermitente y semanal. Presencia de masa a nivel de hipogastrio, de crecimiento lento. Hace 6 días presenta dolor tipo pulsátil con escala de dolor 3 de 10, en región mesogástrica, acompañado de nauseas que no llegan al vómito. Se medica con metoclopramida, con el cual atenúa las náuseas.
Procedente de la ciudad de Sucre, radicada en La Paz, muchos años. Sin antecedentes familiares y no patológicos relevantes. Fue operada hace 4 años de litiasis vesicular.
Antecedentes Ginecológicos: Menarca a los 15 años, Gesta: 0, Partos: 0. Abortos: 0. Ritmo 3-4/28-30 días
Examen Físico General. Presión arterial: 100/60, Frecuencia cardiaca: 69 por minuto, Respiración 18 por minuto, Temperatura 36.5 °C, Peso: 70 kg. Estatura 1,47 m.
Cabeza y cuello normal, Cardiopulmonar normal.
Abdomen globuloso, se observa cicatriz quirúrgica de 2 cm en epigastrio y otra de 2 cm en región supraumbilical de cirugía laparoscópica, blando, depresible, en región de hipogástrico se observa masa tumoral a la palpación de consistencia dura poco móvil de 30 x 20 cm que abarca de hipogastrio a mesogástrico y parte de flanco derecho. RHA (++).
Genitales normales, resto del examen físico normal.
Diagnóstico Clínico: Miomatosis uterina
Laboratorio. Serie Roja: Eritrocitos 5.950.000 ce, Hb 18 g%, V.C.M. 91.5 Uug, Hb.C.M. 30.5 Uug, C.Hb.C.M. 33.3 %, VES 3 en un minuto.
Serie Blanca. Leucocitos 6.100 ce. Segmentados 54%, monocitos 1%, Linfocitos 41%, cayado 1%, basófilosO%.
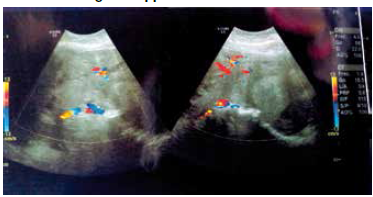
Ecografía. En cavidad abdomino-pélvica se observa masa lobulada heterogénea con áreas de necrosis central y flujo intrínseco Doppler color con patrón de baja resistencia, mide 25 x 9 x 23 cm para un volumen aproximado 2815 ce de probable dependencia uterina sin embargo no se descarta origen ovárico (Fig. 1 y 2)
Útero poco definido, por masa descrita anteriormente, presenta imágenes de ecogencia e hipoecogencias dependientes de su pared anterior. Endometrio no caracterizarle adecuadamente. Ovarios visibles. No se observa liquido libre en cavidad peritoneal ni recesos pélvico.
Impresión Diagnostica: Masa abdomino-pélvica de probable origen uterino, considerar miomatosis uterina, sin embargo, no se descarta origen ovárico.
Fig. 1: Ecografía de masa tumoral
Fig. 2: Doppler de masa tumoral
PROTOCOLO OPERATORIO
Bajo anestesia raquídea se realiza incisión transversal suprapúbica (PFANNENSTIEL), abierta cavidad se observa útero de 8 x 5 x4 cm, a nivel de retroperitoneo se observa tumoración que abarca desde hueco pélvico, flanco derecho y región subhepática.
Se abre ventana en hoja posterior de ligamento ancho,16 se reseca tumor por divulsión digital cuidado órganos retroperitoneales, (uréter, vena cava inferior, pelvis renal y riñon derecho) se obtiene masa tumoral lobulado de aspecto lipomatoso (3000 g), no presenta adherencia a órganos retroperitoneales. Luego se realiza histerectomía total mas ooforectomia bilateral (Fig. 3 y 4)
Diagnostico Postoperatorio: Tumor retroperitoneal, lipoma retroperitoneal, a DC liposarcoma.
Fig. 3: Incisión Pfanietiel
Fig. 4: Tumor retroperitoneal
HISTOPATOLÓGICO
DESCRIPCIÓN MACROSCÓPICA. 1) Útero y anexos que mide 12 cm. cuello con OEC. transversal y entreabierto, canal endocervical permeable, espesor con cavidades quísticas y contienen material gelatinoso, cavidad uterina de 4 X 3 cm. tapizada por endometrio de 0,2 cm., miornetrio engrosado con dos nodulos firmes y delimitados de 0,8 y 2,5 cm., grisáceos y arremolinados. Anexos, con ovarios lobulados de 4 y 4,5 cm. con pequeñas cavidades quísticas corticales y un cuerpo amarillo hemorrágico de 1,8 cm., quiste paratubárico de 1,2 cm. de pared delgada y contenido acuoso (Fig. 5)
2) Como lipomas retroperitoneales, cinco tumores lobulados 6 blandos que varían de 7 hasta 19 cm., superficies bien encapsuladas lisas y café grisáceas, las caras de sección muestran un aspecto fibroticos blanquecinos y arremolinados (Fig. 5)
DESCRIPCIÓN MICROSCÓPICA. 1) Los cortes histológicos revelan cuello uterino con endocervix que muestra lesiones quísticas mucosecretoras y contienen moco con leucocitos. Endometrio con glándulas tortuosas recubiertas por epitelio columnar simple y con vacuolización irregular, estroma edematoso y congestivo. Los nodulos intramurales corresponden a neoplasias mesenquimatosas benignas compuestas por células musculares lisas e hipertrofiadas que se disponen en haces entrecruzados. Los ovarios muestran lesión quística no neoplásicas tapizadas por epitelio cuboidal simple y correspondientes a la granulosa, así como un cuerpo amarilla hipertrófico y hemorrágico. El quiste paratubárico de pared conectiva adelgazada con revestimiento epitelial plano y simple, 2) Los cortes histológicos de los tumores peritoneales revelan, neoplasias mesenquirnatosas benignas compuestas por proliferación de fibras musculares lisas e hipertrofiadas, con núcleos centrales ovales y pignóticos que muestran raras figuras de mitósis, se disponen en gascículos entrelazados e intercalados con fibrosa colágenas gruesas onduladas, se encuentran bien delimitados por cápsula fibrosa.
DIAGNÓSTICO HISTOPATOLÓGICO
1. Útero con endocervicitis crónica con quistes de Naboth. endometrio con signos de hiperestrogenismo.
2. Leiomiomas uterinos íntramurales
3. Ovarios con quistes foliculares y cuerpo amarillo hipertrófico hemorrágico.
4. Leiomiomas peritoneales múltiples.
DISCUSIÓN
La literatura médica indica que un tercio de los tumores malignos localizados en el retroperitoneo son sarcomas, y aproximadamente 15% son sarcomas de tejido blando.17 El liposarcoma es un tumor maligno de origen mesodermico derivado del tejido adiposo, presenta unas características propias en relación con su localizacion profunda y su crecimiento lento y expansivo, alcanzando diámetros medios de 10 a 15 cm, con compromiso de los órganos vecinos hasta en un 80% de los casos.18 La Leiomiomatosis peritoneal es una entidad benigna poco frecuente que se caracteriza por la presencia de numerosos nodulos de músculo liso peritoneales o subperitoneales.19 Se diferencian de los leiomiosarcomas por la ausencia de atipia y actividad mitótica y porque ellos son de localizacion retroperitoneal más frecuente que los leiomiomas, excepto en el área pélvica donde estos últimos tienen la primacía.20
CONCLUSIÓN
En conclusión, los tumores retroperitoneales son tumores raros. Los síntomas difusos y poco específicos generan diagnósticos en estadios avanzados, principalmente por un gran tamaño tumoral (Fig. 6), a pesar de esto, los pacientes con resecciones totales tienen buen resultado. Consideramos que el manejo óptimo de los pacientes inicia desde la sospecha diagnóstica temprana e incluye el uso racional de imágenes como la resonancia magnética, el análisis histológico de las muestras por patólogos con experiencia, la planeación preoperatoria teniendo en cuenta los posibles órganos comprometidos y la decisión de terapias adicionales previas o postoperatorias de acuerdo al tipo y estadio tumoral.
Fig. 5: Pieza quirúrgica

Fig. 6: Extensión del Tumor

REFERENCIAS
1. López, M. López, N. Ferrufino, G. Ferrufino J. Liposarcoma retroperitoneal gigante de novo multifocal. Gaceta Medica Boliviana. Vol. 42, N°.2, 2019:168-171
2. Zuluaga Gómez A, Jiménez Verdejo A. Patología retroperitoneal. Actas Urol Esp, 2002; 26(7):445-66.
3. Tambo M, Fujimoto K, Miyake M, Hoshiyama F, Matsushita C, Hirao Y. Clinicopathological review of 46 primary retroperitoneal tumors. IntJUrol, 2007; 14(9):785-8.
4. An JY, Heo JS, Noh JH, Sohn TS, Nam SJ, Choi SH, et al. Primary malignant retroperitoneal tumors: analysis ofa single institutional experience. EurJSurg Oncol. 2007; 33(3):376-82
5. Campohermoso, O. Anatomía Humana Practica. La Paz: Ed. Original Sam José; 1916
6. Ackerman LV. Tumors of retroperitoneum, mesentery and peritoneum. Atlas of tumor pathology. Armed Forces Institute of Pathology 1954; Sec 6 (23-24):136.
7. Morgagni, J. De sedibus, et causis morborum peranatomen indagatis, Librí quinqué. Venetia Remondinius, 1761.
8. Brugés, R. Tumores retroperitoneales: un diagnóstico y tratamiento complicados. Revista Colombiana de Cancerología. Vol. 19. N° 2. 2015:59-122
9. Virseda, JA. Dónate, MJ. Navarro, HP. Tumores retroperitoneales primarios, revisión de nuestros casos de los diez últimos años. Arch. Esp. Urol. 2010; 63 (1): 13-22
10. Zavala, JC. Tumores retroperitoneales. En: Pérez, E. Gastroenterología. México: Ed. McGraw-Hill Interamericana, 1912, p. 563
11. Swallow, CJ. Catton, CN. Improving outcomes for retroperitoneal sarcomas: a work in progress. Surg Oncol ClinNAm., 21 2012: 317-331
12. Urology. Meredith Campbell. Retroperitoneal Pathology. Edicones en CD Rom Disponible en:
13. Tambo M, Fujimoto K, Miyake M, Hoshiyama F, Matsushita C, Hirao Y. Clinic pathological review of 46 primar/ retroperitoneal tumors. Int J Urol. 2007;14(9):785-788.
14. Enzinger FM, Weiss SW. Soft tissue tumors. 4th ed. ST. Louis, MO: Mosby-Year Book, 2001
15. García, M. Lehmann, C. Ríos, D. Tumores retroperitoneales: experiencia de 11 años en un centro de referencia en canceren un país latinoamericano (2000-2011). Revista Colombiana de Cancerología. Vol. 19 N° 2, 2015:61-70
16. Figueroa, JD. Herazo, F. Ríos, DC. Descripción de dos abordajes quirúrgicos para tumores retroperitoneales, experiencia en el Hospital Pablo Tobón Uribe, 2003-2011. Rev Colomb Cir. 2012; 27:221-226
17. Jacob MS, Patel S, Sasken H, Pérez Y, Katz V, Ingram M. Retroperitoneal liposarcoma: A case report. IJCRI. 2014; 5:108-12.
18. Sánchez, M. Terán, PN. Ferrufino, G. Liposarcoma Retroperitoneal Gigante: A Propósito de un Caso. Rev Cient Cieñe Med 2010; 13(1): 41-3
19. Benitez, H. VAN DER LINDE ROSEMBERG, V. PARRA, R. Leiomiomatosis Peritoneal Diseminada. Int. J. Morphol. Vol.32, n.2, 2014:666-670.
20. Martínez, L. Botello, A. Herrera, Y. Leiomioma Retroperitoneal: presentación de un caso. Revista Habannera de Ciencias Médicas. Vol. 7 n.2, 2008












 uBio
uBio