Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Médica La Paz
versión On-line ISSN 1726-8958
Rev. Méd. La Paz v.20 n.1 La Paz 2014
EDUCACIÓN MÉDICA CONTÍNUA
ELECTROCARDIOGRAFÍA BÁSICA EN LAS UNIDADES DE CUIDADOS INTENSIVOS
*Dr. Oscar Vera Carrasco
* Especialista en Medicina Crítica y Terapia Intensiva. Profesor Emérito de Pre y Postgrado de la Facultad de Medicina de la Universidad Mayor de San Andrés (UMSA). Ex Jefe del Departamento de Terapia Intensiva del Instituto Nacional de Tórax-Bolivia.
INTRODUCCIÓN
La atención del paciente en estado crítico es compleja, ya que los mecanismos fisiológicos que regulan una o varias funciones biológicas se encuentran habitualmente deterioradas y son disfuncionantes. Como consecuencia de esto, es fácil observar en estos pacientes la interrelación existente entre los diversos sistemas orgánicos y los efectos de la fisiopatología celular sobre todos ellos.
El corazón, no se encuentra exento de verse inmerso en este complejo entramado de interrelaciones, pudiéndose observar con frecuencia los efectos de estas alteraciones sobre sus funciones contráctiles y eléctricas. El electrocardiograma (ECG) nos puede servir como instrumento de orientación diagnóstica en muchas de estas alteraciones y como herramienta capaz de evaluar su evolución.
En este artículo se revisa los trastornos electrocardiográficos frecuentemente observados en la práctica clínica, como son las arrítmias, y los efectos de las alteraciones electrolíticas, de algunos fármacos, tóxicos y otras de origen no cardiaco, los mismos que con una adecuada interpretación, y basadas en las manifestaciones clínicas y de laboratorio, pueden orientar los diagnósticos precisos para su manejo correcto.
ARRÍTMIAS CARDIACAS
La presentación de arrítmias en los pacientes graves depende de dos tipos de factores fundamentales: los mecanismos patogénicos intrínsecos de cada arrítmia y una serie de factores favorecedores o desencadenantes.
En principio, ante cualquier alteración del ritmo cardiaco debemos plantearnos las siguientes interrogantes:
¿Cuál es el riesgo vital inmediato de la arrítmia?
¿Qué repercusión hemodinámica presenta?
¿Es posible identificar y tratar la causa?
¿Es necesario iniciar medidas terapéuticas inmediatas?
¿El tratamiento puede conllevar complicaciones derivadas de efectos secundarios o indeseables?
¿Cuál es el pronóstico del proceso global, incluyendo la patología aguda actual y los procesos de base que pueden influir como fenómenos desencadenantes?
Luego del análisis de la situación desde todas estas perspectivas, será posible hacer un enfoque global del problema y plantear su solución de la mejor forma, ya que muchas de las arrítmias no son más que la expresión de otros trastornos fisiopatológicos, y la solución probablemente no sea tratar la arrítmia, sino la causa desencadenante.
Clasificación
Con un objetivo didáctico se clasificará las arrítmias de la siguiente forma:
Por su frecuencia:
Ritmos lentos (< 60 lat./min.) o bradiarrítmias
Ritmos rápidos (> 100 lat./min.) o taquiarrítmias
Por su ritmicidad
Rítmicas
Arrítmicas
Por su origen:
Supraventriculares (complejo QRS estrecho)
Ventriculares (complejo QRS ancho)
- Ritmos lentos o bradiarrítmias
Son aquellos que mantienen una frecuencia cardiaca por debajo de 60 latidos por minuto. De ellos los más frecuentes son la bradicardia sinusal, el bloqueo sinoauricular y el bloqueo aurículoventricular, destacando la patología del seno y las alteraciones de la conducción aurículoventricular (AV) por la posibilidad de generar problemas con repercusión significativa en el paciente.
- Bradicardia sinusal
Es aquel ritmo de origen sinusal y frecuencia inferior a 60 latidos por minuto. Es prototipo de individuos entrenados, jóvenes y con predominio del tono vagal. En pacientes de edad avanzada, la bradicardia puede sugerir disfunción del nódulo sinusal, en especial si es persistente y no existe elevación de la frecuencia con el ejercicio ni la atropina por vía intravenosa. Otras posibles causas son las siguientes: enfermedad del nodo (síndrome bradicardia-taquicardia), hipotiroidismo, hipertensión intracraneal, patología carotidea, fármacos bradicardizantes (bloquenates beta adrenérgicos, digoxina, etc).
- Paro sinusal
Es consecuencia de la falta de formación del impulso en el nódulo sinusal, por un trastorno del automatismo, lo que se manifiesta en el ECG por la ausencia de las ondas P. Es producido por un tono vagal incrementado o hipersensibilidad del seno carotideo, y suele asociarse a arrítmia sinusal.
- Ritmos de escape
Son consecuencia de una disminución del automatismo sinusal o bien de la imposibilidad de la conducción del impulso a nivel sinoauricular o aurículoventricular.
- En los casos de los ritmos de escape nodal, la frecuencia oscila entre 40 y 60 latidos por minuto y el QRS es estrecho, en ocasiones seguido de onda P retrógada; en otros casos, la onda P no es visible por estar incluida en el QRS.
- Si la onda P no es retrógrada, pero es diferente a la sinusal y precede al QRS, puede deberse a un ritmo de escape auricular. Los ritmos de escape ventriculares o idioventriculares muestran frecuencias por debajo de 40 latidos por minuto y el QRS es ancho y mellado, tanto más cuanto más bajo es su origen ventricular.
Los ritmos de escape son un mecanismo de suplencia cuando existe un fracaso del automatismo o de la conducción, y su diagnóstico orienta sobre la existencia de estos trastornos.
- Bloqueo sinoauricualar
Es consecuencia de un trastorno en la conducción del impulso desde el nódulo sinusal a la aurícula. Se distinguen clásicamente en tres grados:
- Bloqueo sinoauricular de primer grado: es consecuencia de la prolongación del tiempo de conducción desde el nódulo sinusal a la aurícula, y su diagnóstico por el ECG de superficie no es posible. Para su diagnóstico precisaría el registro endocavitario directo del potencial del nódulo sinusal.
- Bloqueo sinoauricular de segundo grado: se pueden distinguir dos tipos:
* El tipo I o de Wenkebach, en el que se comprueba en el ECG acortamiento progresivo de los intervalos PP, hasta producirse una pausa que es menor del doble del intervalo PP, siendo el PP que precede a la pausa menor que el intervalo que la sigue.
* El tipo II, es aquel en el que las pausas son múltiplos del intervalo PP, y en ocasiones se expresa por una bradicardia sinusal extrema, que es seguida por una frecuencia doble a la previa (bloqueo sinoauricular 2:1).
- Bloqueo sinoauricular de tercer grado o completo: supone la interrupción entre el nódulo sinusal y la aurícula, por lo que en el ECG se objetivará la presencia de un ritmo de base distinto al sinusal (nodal, auricular bajo, etc.).
- Bloqueo aurículoventricular
Las alteraciones de la conducción AV pueden afectar a cualquier nivel del sistema de conducción, y desde el punto de vista electrocardiográfico se clasifican en tres grados, que se pueden aplicar a cualquier nivel de localización. Se describe como suprahisiano, intrahisiano o infrahisiano.
- Bloqueo AV de primer grado: en este bloqueo AV (BAV) se observa un retraso en el paso del estímulo a través del nodo AV, lo que se traducirá en una prolongación del intervalo PR mayor de 0,18 segundos en el niño, 0,20 segundos en el adulto y 0,22 segundos en el anciano. Los intervalos PR serán siempre constantes. El ECG será rítmico.

- Bloqueo AV de segundo grado: en este trastorno se observa como algunas ondas P no se transmiten a los ventrículos a pesar de haberse superado el periodo refractario fisiológico de la unión AV. Existen dos tipos de BAV de segundo grado:
* Mobitz I o de Wenckebach: en este bloqueo se observa un incremento progresivo en la duración del intervalo PR hasta que una onda P no se conduce al ventrículo. El ECG mostrará un complejo QRS arrítmico.
* Mobitz II: en este caso los intervalos PR son constantes (no existe prolongación de PR), pero ocurre que ocasionalmente se produce un agotamiento de la capacidad de conducción del nodo AV y no transmite el estímulo, fallando el complejo QRS; por lo tanto el ECG también será arrítmico)
Un tipo especial de BAV de segundo grado es el tipo 2:1, en el que una onda P se transmite a los ventrículos y otra no. No es posible definir si el mecanismo es el de un Mobitz I o el de un Mobitz II, diferenciándose de modo dudoso en que si el complejo QRS es estrecho, el mecanismo original probablemente es el tipo I, mientras que si es un complejo QRS ancho, el mecanismo será de tipo II, ya que implica un grado severo de afectación del sistema de conducción.

- Bloqueo AV de tercer grado: existe una disociación completo entre las ondas P y los complejos QRS. El ritmo auricular nunca sobrepasa el nodo AV, apareciendo un ritmo ventricular de rescate. El ECG registrará un QRS rítmico, que podrá ser estrecho o ancho según el nivel donde se produzca.
- Alteraciones de la conducción intraventricular
- Bloqueo completo de la rama derecha del haz de his
* Duración del complejo QRS mayor o igual a 0.12 s
* Complejos rSR en V1, con ondas T que se oponen a la dirección eléctrica del complejo QRS en derivaciones derechas y positivas en el resto.
* La onda S puede ser sólo una muesca o incluso no aparecer y expresar complejos R en V1.
* Eje del complejo QRS desviado a la derecha.

- Bloqueo completo de la rama izquierda del haz de his
* Complejo QRS de amplitud superior al rango normal (≥ 0.12s).
* Complejos QS o rS en V1 con onda S ancha y profunda.
* En DI y V6 se pierde la onda Q del primer vector septal y se registra una onda R empastada con una muesca en su rama ascendente.
* El segmento ST y la onda T suelen dirigirse en sentido contrario al complejo QRS.
* El eje del complejo QRS suele hiperdesviarse a la izquierda.

- Hemibloqueo anteriosuperior izquierdo
* Duración del complejo menor de 0.12 s, habitualmente normal.
* Onda R dominante en DI con o sin onda Q inicial.
* Complejos RS en DII, DIII y aVF.
* S III mayor que S II y R II mayor que R III.
* Complejo qR en aVR.
* AQRS desviado a la izquierda entre -45° y -90°
* La repolarización ventricular no suele alterarse de modo significativo.

- Hemibloqueo pósteroinferior izquierdo
* Duración del complejo QRS menor de 0.12 s, habitualmente normal.
* AQRS desviado a la derecha entre +90° y +120°
* Complejos RS en DI y aVL
* Ondas Q en cara inferior (II, III y aVF), estrechas y seguidas de una onda R prominente.
* R III mayor que R II
* No suelen apreciarse alteraciones de la repolarización ventricular.

Ritmos rápidos o taquiarrítmias
Una forma práctica de clasificación puede ser:
- Taquicardias de complejo QRS estrecho: rítmicas y arrítmicas.
- Taquicardias de complejo QRS ancho: rítmicas y arrítmicas.
Taquicardias de complejo QRS estrecho: son aquellas cuya frecuencia ventricular excede los 100 lat./min. Si el complejo QRS es estrecho (< 0,12 s), se considera que su origen es supraventricular (por encima de la bifurcación del haz de his.
Taquicardias de complejo QRS estrecho rítmicas
- Taquicardia sinusal: frecuencia cardiaca mayor de 100 lat./min., con presencia de ondas P previas a todos los complejos QRS. Deberá diagnosticarse en un paciente sometido a estrés físico-psíquico que presente una frecuencia en reposo mayor de 100 y menor de 150 lat./min., con ondas P sinusales (P+ en I, II y III), con relación P: QRS 1:1, y que responde a maniobras vagales con enlentecimiento progresivo pero transitorio.

- Enfermedad del nodo sinusal: patología en la que se puede encontrar alteraciones variables en la frecuencia del nodo sinusal, con taquicardias paroxísticas seguidas de periodos de bradicardia patológica; paradas sinusales o bloqueos sinoauriculares, etc.
- Taquicardia supraventricular paroxística (TSVP): taquicardia que se caracteriza por su presentación paroxística, de inicio y terminación rápida. Su diagnóstico se basa en la frecuencia ventricular, generalmente superior a 150 lat./min. y ausencia de ondas P por encontrarse englobadas en el complejo QRS. De apreciarse la actividad auricular, se encontrarían tras el complejo QRS (ondas P retrógradas).
Es frecuente su aparición en jóvenes, sin patología estructural, y la respuesta a los estímulos vagales sigue la ley del todo o nada, es decir, desaparecen súbitamente con maniobras vagales o no se modifica.
- Flúter auricular: se trata de una TSV de alta frecuencia (200-400 lat./ min.), originada por un mecanismo de reentrada con un grado de bloqueo variable (P: QRS 2:1, 3:1, etc.). En el ECG no se observan ondas P, sino, ondas con morfología en dientes de sierra llamadas ondas F. Es muy habitual la presentación del flúter con frecuencia auricular a 300 lat./min. y una conducción a los ventrículos con bloqueo 2:1, por lo que observaremos una TSV rítmica a 150 lat./min., con ondas F (flúter común).
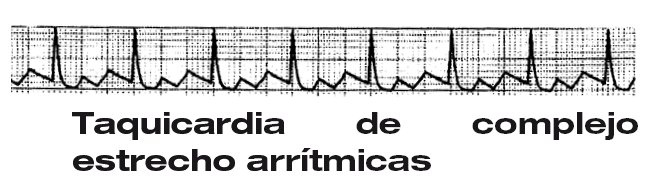
- Complejos auriculares prematuros (extrasístoles auriculares): es un ritmo cardiaco normal con la sobreimposición de latidos supraventriculares (complejo QRS estrecho) procedentes de la despolarización de otro foco auricular o, más raramente, focos nodales o hisianos. En el ECG destaca la presencia de ondas P (no sinusales) que se intercalan en un ritmo sinusal normal. Si el intervalo R-P es corto, habitualmente se siguen de un P-R largo. La extrasistolia supraventricular no debe ser tratada si es asintomática (tratar la patología de base causal).

- Taquicardia auricular multiforme: se produce por activación auricular desde múltiples focos irritativos, con diferentes frecuencias de descarga. El ECG es anárquico, con complejos QRS estrechos, pero precedidos todos de onda P con diferentes morfologías (sinusales y no sinusales). Este registro se observa en pacientes con EPOC o con insuficiencia cardiaca congestiva. Se considera la antesala de la fibrilación auricular.

- Fibrilación auricular: se observa la aparición de múltiples focos auriculares de despolarización por reentradas que condicionan una desorganización completa de la contractilidad auricular, y que se conduce a los ventrículos de modo variable. No se ven ondas P sino ondas f con una frecuencia entre 400 y 600 lat./min. La respuesta ventricular suele ser totalmente irregular, con frecuencias variables en función del grado de BAV presente. Las maniobras vagales condicionan un enlentecimiento progresivo y transitorio de la frecuencia cardiaca, pero manteniendo la irregularidad de los intervalos R-R.

- Taquicardias de complejo QRS ancho
Son aquellas que presentan una frecuencia ventricular superior a 100 la./min y amplitud del complejo QRS mayor de 0,12 s. Suelen asociarse casi en su totalidad con patología estructural, generalmente cardiopatía isquémica.
El ECG muestra: complejos monofórmicos o polimórficos, taquicardia regular o irregular, presencia de ondas P y relación P-QRS; análisis del complejo QRS. Suelen deberse a un origen ventricular de los estímulos, pero también es posible un origen supraventricular en casos de bloqueo de rama estructural preexistente o funcional (aberrancia), o en casos de conducción a través de una vía anómala.
- Taquicardias de complejo QRS ancho monomórficas
Se distinguen fundamentalmente tres posibilidades:
- Taquicardia ventricular: se define como la sucesión encadenada de tres o más latidos cardiacos, con una frecuencia superior a 100 latidos/minuto, originados por debajo de la bifurcación del haz de His. Dependiendo de su duración y repercusión clínica, las podemos diferenciar en TV sostenidas (duración > 30 seg. o que requieren maniobra urgentes para su control) y TV no sostenidas (autolimitadas < 30 seg.).
El mecanismo arritmógeno puede ser cualquiera de los habituales: incremento de la excitabilidad miocárdica ventricular o fenómenos de reentrada. Los siguientes signos electrocardiográficos sugieren el origen ventricular de esta arrítmia:
1. Complejo QRS ancho (> 0,14 seg.) durante la taquicardia.
2. Disociación AV (las aurículas se despolarizan por el nodo sinusal y los ventrículos por el foco ectópico, con frecuencias diferentes). Este fenómeno sólo se ve en un 25% de los casos, pero es diagnóstico en caso de presentarse.
3. Presencia de latidos de fusión y capturas supraventriculares.
4. Patrón concordante (complejo QRS predominantemente positivos o negativos en todas las derivaciones).
5. En caso de preexistir un bloqueo de rama en el ECG normal, es sugestivo de origen ventricular la aparición de bloqueo de rama contralateral durante la taquicardia, aunque mantener el mismo tipo de bloqueo no excluye el origen ventricular.
6. Desviación del eje frontal del complejo QRS al cuadrante superior derecho (S1, S2, S3).
7. Criterios morfológicos del complejo QRS: si la taquicardia tiene morfología de bloqueo de la rama derecha (complejo QRS predominantemente positivo en V1) pero pensaríamos en una TV si el complejo QRS en V1 es de tipo monofásico R o bifásico RS o V6 se describe como R menor que S o QS. Si presenta morfología de bloqueo de rama izquierda (complejo QRS predominantemente negativo en V1) se sospecha TV si R en V1, es mayor de 0,04 seg. o complejos qR o RS en V6.
- TSV con bloqueo de rama: la activación de los ventrículos se realiza a través de las vías de conducción ordinarias pero bloqueo de rama secundario a la taquicardia (mecanismo de agotamiento) o por daño estructural. El complejo QRS será ancho, aunque menos que el originado en el ventrículo (< 140 ms), y con el componente inicial rápido (inicio R-nadir S<100 ms).
Característicamente presentará el siguiente ECG:
1. Complejo QRS menor de 140 ms.
2. Asociación AV con relación P: QRS dependiente del tipo de taquicardia basal (2:1 para flúter o 1:1 paralaTSVP).
3. R-R regular en caso de flúter o TSV, o irregular en caso de AC x FA.
4. Ausencia de latidos de fusión o capturas.
5. Patrón no concordante con TV ni presencia de bloqueos de rama cambiantes durante la taquicardia.
6. Respuesta a las maniobras clínicas o farmacológicas de bloqueo nodal.
- TPSV con preexcitación: se produce por la presencia de un ritmo rápido supraventricular que se conduce a los ventrículos a través de una vía accesoria anterógrada, o por una reentrada antidrómica (aurícula vía accesoria ventrículos sistema de conducción aurículas.
Características del ECG:
1. Complejo QRS mayor de 140 ms.
2. Asociación AV.
3. Regularidad de R-R (si el ritmo de base es una fibrilación auricular, los intervalos R-R serán irregulares).
4. Ausencia de latidos de fusión o capturas (no confundir las capturas con latidos conducidos a través del sistema específico de conducción de modo correcto).
5. Patrón de WPW en ECG basal, de similares características que el observado durante la taquicardia.
6. Patrón concordante y morfología de TV, ya que la despolarización será semejante a la TV (se pueden diferenciar por la presencia de complejos QS o QRS en V6 de la TV, que no se observarán en estas TSV, ya que la despolarización de los ventrículos siempre se dirige de arriba abajo y originará ondas de despolarización positivas en V6.
7. Respuesta a maniobras vagales o bloqueo farmacológico.

- Taquicardias de complejo QRS ancho polimórficas
- Fibrilación auricular con preexcitación: se observa complejos QRS anchos, con morfología y duración variables debido a la despolarización ventricular a través de la vía anómala y a través del sistema específico de conducción, que generará diversos grados de fusión entre los dos frentes de despolarización.
- TV polimorfa: es la taquicardia originada por la presencia de múltiples focos irritativos ventriculares que descargan con intervalos diferentes, dando lugar a un registro electrocardiográfico con complejos QRS anchos, polimorfos y con intervalos RR cambiantes. El patrón de semejanza de los complejos estará muy alterado (diagnóstico diferencial) con la fibrilación auricular conducida con aberrancia.
Está asociada frecuentemente con fenómenos inflamatorios miocárdicos, cardiopatía isquémica, fármacos o trastornos electrolíticos.
- Torsade de pointes o Torción de puntas: taquicardia polimórfica caracterizada por presentar complejos QRS anchos, de amplitud y dirección del eje variables siguiendo un patrón helicoidal. Por regla general se asocian a síndromes con QT largo, tanto congénitos como adquiridos por alteraciones electrolíticas, fármacos, etc. Habitualmente se presenta de forma paroxística, autolimitada, alternando con fases de ritmo sinusal, pero se mantiene de forma prolongada, degenera en fibrilación ventricular.

- Síndrome de Brugada: presencia de TV polimórficas no sostenidas en pacientes sin cardiopatía estructural, que presenta característicamente en el ECG basal bloqueo completo de la rama derecha y elevación del segmento ST en V1-V3. Estos pacientes tienen un alto riesgo de muerte súbita por degeneración de la taquicardia en FV, por lo que son subsidiarios de implantación de un desfibrilador automático preventivo.
- Fibrilación ventricular
(FV): es el resultado de la desorganización completa de la actividad eléctrica ventricular, con la aparición de infinitos focos de despolarización que inducen una falta de contracción muscular efectiva y la muerte del paciente. Electrocardiográficamente se observa un registro anárquico, de ondas irregulares, con tamaño conservado en un primer momento y que progresivamente tenderán a hacerse finas hasta llegar a la asistolia.

La FV puede aparecer como fenómeno arrítmico primario o como degeneración de TV sostenida. Su presencia es equivalente a la ausencia de pulso eficaz y fallecimiento del paciente, por lo que su tratamiento debe ser inmediato mediante choques eléctricos, intentando una despolarización global de todo el miocardio y el reinicio de un ritmo efectivo.
TRASTORNOS ELECTROLÍTICOS
Potasio
El Potasio tiene un rol importante en la función de las células del organismo. En el corazón, los niveles de potasio intracelular y extracelular son esenciales para la norma! generación y conducción del impulso eléctrico. Trastornos eléctricos que pueden terminar en fibrilación ventricular o asistolia pueden presentarse en pacientes con hiperkalemia severa. Los cambios iniciales en la hiperkalemia se caracterizan por aparición de ondas T picudas, en "tienda de campaña", y acortamiento del intervalo Q-T que refleja una polarización anormalmente rápida. Estas ondas pueden confundirse con las ondas T altas que aparecen en la isquemia miocárdica temprana (subendocárdica). Sin embargo, estas últimas se asocian a un intervalo Q-T prolongado o normal. Ver las siguientes figuras.

Tomado de Reig-Valero R, Oltra-Chorda R. Electrocardiografía básica. En: Tejeda Adell. El paciente agudo grave. Barcelona (España). Masson 2005, Modificado.
A mayores niveles séricos de potasio (> 7 mEq/L) el ECG muestra cambios que reflejan una despolarización retardada: complejos QRS anchos (manifestación de retardo en la despolarización ventricular), descenso en la amplitud, hasta la eventual desaparición de la onda P. También puede presentarse Bloqueo A-V de segundo y tercer grado. El segmento S-T puede mostrar un supradesnivel en V1 y V2; este supradesnivel simula un infarto agudo de miocardio de localización septal y ha sido descrito como "corriente de injuria dializable".
Esta imagen de pseudo IAM, además de estar acompañada por las manifestaciones electrocardiográficas ya descritas en la hiperkalemia (T picuda, QRS ancho, etc), presenta el segmento S-T supradesnivelado con una pendiente descendente que refleja el gradiente eléctrico producido por la despolarización no homogénea de diferentes porciones del miocardio. Ver la figura siguiente.

Los cambios en el ECG presentes en la hipokalemia se deben a un retardo en la repolarización. El segmento S-T se deprime, la onda T disminuye en su amplitud o aparece invertiday la onda U es más evidente. En casos severos puede ocurrir aumento de la amplitud de la onda P y el intervalo P-R se prolonga.

Tomado de Reig-Valero R, Oltra-Chorda R. Electrocardiografía básica. En: Tejeda Adell. El paciente agudo grave. Barcelona (España). Masson 2005, Modificado.
La hipokalemia tiende a prolongar el intervalo Q-T; también favorece la aparición de arritmias por reentrada al retrasar la despolarización. Además, puede condicionar arritmias por aumento del automatismo; este riesgo aumenta en pacientes que utilizan digoxina o presentan isquemia de miocardio.
Calcio
El calcio es determinante para la duración de la fase 2 (apertura de canales lentos de calcio) del potencial de acción. La hipercalcemia puede acortar y la hipocalcemia prolongar el intervalo Q-T a expensas del segmento S-T. Ver la figura siguiente.
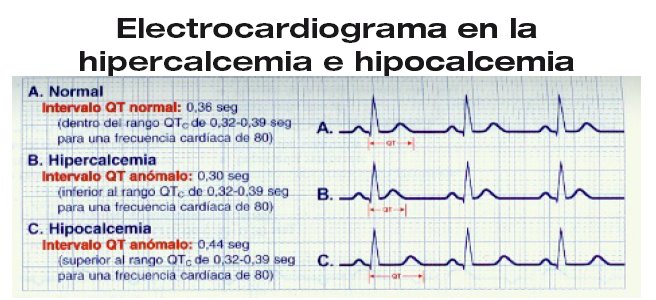
Tomado de Reig-Valero R, Oltra-Chorda R. Electrocardiografía básica. En: Tejeda Adell. El paciente agudo grave. Barcelona (España). Masson 2005, Modificado.
En la hipercalcemia severa también se observa prolongación del QRS y del P-R, hasta bloqueo A-V. La combinación de Q-T prolongado y ondas T en tienda de campaña refleja hipocalcemia e hiperkalemia, asociación frecuente en pacientes con Insuficiencia renal crónica en los que la hipocalcemia se desarrolla por trastornos en el metabolismo del calcio y la vitamina D y, la hiperkalemia por alteraciones en el filtrado glomerular y acidosis metabólica.
Magnesio
La hipomagnesemia habitualmente acompaña a la hipokalemia y no parece producir cambios específicos en el ECG. El magnesio es importante para mantener la concentración de potasio intracelular y mantener la estabilidad eléctrica de la célula cardiaca. La hipermagnesemia aislada tampoco es una condición frecuente, puede presentarse en pacientes con Insuficiencia renal que también presentan otras alteraciones electrolíticas. Las alteraciones electrocardiográficas derivadas de ambas posibilidades son similares a las producidas por el potasio, tanto por exceso como por defecto. El magnesio también se utiliza como atiarrítmico en la taquicardia polimorfa o "torsade de pointes".
Sodio
La hiponatremia y la hipernatremia aislada no tienen efectos sobre el ECG. Aunque en pacientes con trastornos de la conducción intraventricular causadas por hiperkalemia la hiponatremia puede prolongar la duración del complejo QRS, mientras que la hipernatremia puede acortar la duración del QRS.
Tromboembolismo Pulmonar (TEP)
Desde la descripción del patrón clásico S1 Q3 T3, el papel del ECG en el TEP agudo continúa siendo de interés. Ver las siguientes figuras.

Tromboembolismo pulmonar agudo
En la fase aguda del TEP pueden ocurrir diferentes cambios en el ECG. Estos incluyen arritmias, trastornos de conducción, cambios en el eje del QRS, cambios en la morfología de la onda P, del complejo QRS, del segmento ST y de la onda T. Estos cambios son extremadamente variables y con poca sensibilidad y especificidad; el ECG puede resultar normal en 25 a 30 % de los casos. Además; la presencia de enfermedad cardiopulmonar preexistente puede simular los cambios descritos en el TEP, disminuyendo la especificidad de este examen. En el TEP se han descrito cambios electrocardiográficos que pueden simular isquemia anteroseptal.
Se han propuesto varios factores para explicar los cambios electrocardiográficos de isquemia de miocardio durante el TEP como ser: 1. La hipertensión auricular severa que impide el drenaje al seno coronario de las venas de Tebesio. 2. La distensión de las arterias que es capaz de desencadenar un reflejo "pulmocoronario". 3. Descenso real del flujo coronario debido al bloqueo circulatorio pulmonar y reducción del volumen minuto sistémico y coronario.
En conclusión, el rol del ECG como un marcador independiente de diagnóstico, severidad y pronóstico en el TEP es limitado; no existe un patrón etectrocardiográfico que permita el diagnóstico inequívoco de TEP, pero la combinación de los datos del ECG más el contexto clínico pueden elevar el grado de sospecha y el diagnóstico puede confirmarse por exámenes más específicos. En años recientes se ha estado evaluando el papel de nuevas técnicas como la ecocardiografía y la Tomografía helicoidal como contribución respecto a la gammagrafía pulmonar y al cateterismo derecho.

Trastornos del Sistema Nervioso Central y Periférico
La asociación de cambios en el ECG con trastornos del SNC ha sido descrita hace más de cinco décadas. Estos ocurren principalmente en sujetos con hemorragia subaracnoidea, pero también pueden estar presentes en la hemorragia intracraneal, trauma craneal, procedimientos neuroquirúrgicos, meningitis, tumores intracraneanos y epilepsia.
Los trastornos del SNC habitualmente causan anormalidades en la repolarización ventricular. Los hallazgos más frecuentes son la depresión del segmento S-T, ondas T aplanadas o invertidas, onda U prominente, presencia de ondas Q y prolongación del intervalo Q-T, este último se asocia a riesgo aumentado (hasta 4%) de taquicardia ventricular polimorfa (torsión de puntas). La prevalencia de estos hallazgos es de 50 a 90%. Estos cambios en el ECG son similares a los que se observan en el síndrome coronario agudo (infarto agudo de miocardio ó angina inestable). Ver la figura siguiente.

Derivaciones precordiales (V1 a V6) y de cara lateral (DI y aVL) en un paciente con hemorragia subaracnoidea.
Además el Q-Tc se encuentra prolongado 613 milisegundos.
Pueden ser transitorios o permanecer hasta 8 semanas. Además pueden presentarse arritmias hasta en 75% de pacientes con enfermedades neurológicas intracraneales, la bradicardia o taquicardia sinusal y las extrasístoles auriculares y ventriculares son frecuentes; rara vez aparecen arritmias significativas. La fibrilación auricular reciente se ha reportado hasta en un tercio de los pacientes con accidente vascular cerebral (AVC), aunque en muchos casos, es difícil establecer si la fibrilación auricular está asociada al AVC ó si es causa o efecto del AVC.
La fisiopatología de estos cambios en el ECG no está del todo definida, y se han propuesto diferentes mecanismos. Existe evidencia de injuria miocárdica en autopsias y reportes de anomalías de la motilidad segmentaría del ventrículo izquierdo observadas por ecocardiografía bidimensional o ventriculografía. En un reporte reciente se confirmó el daño miocárdico con el hallazgo de niveles de troponina I elevados en un grupo de pacientes con enfermedad neurológica aguda.
Pero ¿Cómo la enfermedad del SNC da lugar a injuria miocárdica? Se ha postulado que el daño del SNC puede condicionar una producción excesiva de catecolaminas. Los sitios de regulación simpática en el SNC se hallan en la corteza insular, la amígdala y el hipotálamo lateral.
En pacientes con AVC, en los que la probabilidad de enfermedad coronaria concomitante es elevada, es posible un tono simpático elevado, con el consecuente aumento de la demanda de oxigeno conduzca a daño miocárdico. Sin embargo, también se han encontrado datos de lesión miocárdica en pacientes con coronarias normales, sujetos jóvenes víctimas de accidentes que presentaban hemorragia subaracnoidea. Estas lesiones son similares a las de sujetos con feocromocitoma o consumidores de cocaína. Probablemente las catecolaminas ejercen un efecto tóxico directo sobre las células miocárdicas o median un efecto vasoconstrictor sobre las coronarias.
En un número importante de pacientes con cambios electrocardiográficos, no hay evidencia de daño miocárdico, y estos cambios descritos parecen reflejar cambios electrofisiológicos transitorios.
El síndrome de Guillain Barré, una polirradículoneuritis desmielinizante inflamatoria que afecta a las raíces nerviosas, los pares craneales y nervios periféricos, es otra de las neuropatías que puede causar alteraciones cardiológicas. Estas últimas, si bien son poco frecuentes, pueden ser graves y comprometer la vida del paciente. Se producen por disfunción autonómica en el seno de la neuropatía y puede detectarse con los tests de función autonómica.
En el ECG puede observarse depresión del segmento ST, onda alta, aplanada o invertida e intervalo QT prolongado. Los trastornos más graves son bradiarrítmias (paro sinusal o bloqueo cardiaco), taquiarrítmias (auriculares o ventriculares) y asistolia, que puede ser causa de muerte súbita. Por todo ello, se recomienda la monitorización de los pacientes y en ocasiones ha sido preciso un marcapasos profiláctico. Las alteraciones cardiacas son reversibles.
Trastornos esofágicos
El dolor torácico de origen esofágico es, con frecuencia, difícil de distinguir del dolor de origen cardiaco y, responde de igual manera al uso de nitroglicerina. Esta similitud se explica por la convergencia de señales aferentes del corazón y del esófago a las mismas neuronas del asta dorsal de la médula espinal.
Un 10 a 50% de los pacientes que son referidos a coronariografía por dolor precordial tienen coronarias normales. Hasta un 60% de los casos de dolor precordial de causa no cardiaca pueden tener origen en el esófago. Se ha planteado la hipótesis de que el dolor podría relacionarse con espasmo de las arterias coronarias causado por acetilcolina.
La Enfermedad por reflujo gastroesofágico, muy por encima de los desórdenes de la motilidad esofágica, es la causa más importante de dolor similar a la angina de pecho. La instilación de ácido en el esófago podría generar una descarga simpática que aumente las demandas de oxígeno y producir angina de pecho en pacientes con enfermedad coronaria. Sin embargo, muchos episodios de dolor precordial no se asocian a reflujo ácido ni signos de isquemia en el ECG, y el dolor rara vez es precedido por un episodio de reflujo de acuerdo con estudios de manometría y registro ECG.
Hipotermia
La hipotermia accidental no es infrecuente en regiones frías y, es motivo de más de 1000 muertes anuales y más de 4000 hospitalizaciones.
El ECG muestra cambios característicos en la hipotermia que ayudan a un rápido diagnóstico. La onda J de Osborn es el dato más llamativo. Se trata de una imagen similar a una joroba entre el complejo QRS y la parte inicial del segmento S-T (Ver la siguiente figura), es más notoria en las derivaciones que enfrentan al ventrículo izquierdo (V5, V6 , DI y aVL) y la cara inferior del corazón (Dll, Dlll, aVF). La amplitud de la onda J de Osborn disminuye con el recalentamiento y puede persistir 12 a 24 horas después de la restauración de la temperatura corporal. La onda J es causada por un importante gradiente transmural de voltaje mellado en el epicardio pero no en el endocardio. Esta melladura en el potencial de acción se explica por una corriente de potasio más prolongada en el epicardio que en el endocardio.

Un trazo similar al descrito en la onda J de Osborn también puede presentarse en sujetos jóvenes (especialmente de raza negra) con el síndrome de repolarización precoz, sin que se encuentre enfermedad cardiaca.
En la hipotermia también aparecen artefactos por el temblor muscular (que puede no ser clínicamente evidente), bradicardia sinusal, QRS ancho, prolongación del intervalo P-R y del intervalo Q-T. Puede aparecer fibrilación auricular con una temperatura menor a 32°C y el riesgo de fibrilación ventricular es elevado cuando la temperatura corporal desciende más de 28°C.
Reacciones adversas a medicamentos
Diversos fármacos utilizados en patología cardiaca o no cardiaca pueden causar alteraciones electrocardiográficas. Muchos antiarrítmicos pueden producir complicaciones o efectos proarrítmicos al prolongar el intervalo QT en ciertos individuos predispuestos, o al deprimir la conducción y promover la reentrada. En los últimos años se ha informado casos de Torsade de pointes (taquicardia helicoidal o torsión de puntas), síncope o paro cardiaco durante la terapia con antihistamínicos, antibióticos, procinéticos y otros fármacos con potencial proarrítmico.
La taquicardia helicoidal o torsade de pointes clásicamente descrita como una taquicardia ventricular polimorfa pausa dependiente, ocurre en pacientes portadores del Síndrome de prolongación del intervalo QT (IQTS). El IQTS es un trastorno de la repolarización cardiaca que se caracteriza por la prolongación del intervalo QTc; puede ser adquirido, o consistir en una anomalía congénita. La adquirida está casi siempre asociada a fármacos que prolongan el intervalo QT, aunque también puede deberse a cardiopatía isquémica aguda, desequilibrios electrolíticos, bradicardia extrema por bloqueo AV completo, bloqueo sinoauricular o bradicadia sinusal.
Los principales fármacos que pueden producir el Síndrome de prolongación del intervalo QT, cuyo mecanismo es el bloqueo de los canales de calcio, son los siguientes: eritromicina, grepafloxacina, moxifloxacina, pentamidina, amantadina, cloroquina, sulfametoxazol-trimetoprima, fenotiazinas, haloperidol, antidepresivos tricíclicos, astemizol, terfenadina, ketoconazol, itraconazol, cisaprida, pentamidina, ketanserina, probucol y papaverina.

Intoxicaciones
La cardiotoxicidad es un hallazgo frecuente en pacientes que han sido expuestos a una amplia variedad de agentes tóxicos. Entre los que producen alteraciones electrocardiográficas se pueden incluir a los siguientes: monóxido de carbono, cianuro y organofosforados.
Monóxido de carbono
La intoxicación por monóxido de carbono (CO) es una de las causas más frecuentes de una intoxicación aguda. Los efectos tóxicos del CO son el resultado de la hipoxia tisular. Por lo tanto, las alteraciones electrocardiográficas más comunes que produce en el segmento ST y onda T son la expresión de un déficit a nivel de la célula miocárdica, y frecuentemente acompañadas por evidencias bioquímicas y patológicas de necrosis.
Organofosforados
Los organofosforados por acumulación de acetilcolina producen inicialmente estimulación y luego agotamiento de la transmisión a nivel de la sinapsis colinérgica. La toxicidad producida por estos agentes es consecuencia de la acción muscarínica y nicotínica. Entre las complicaciones cardiacas de intoxicación están presentes la bradicardia seguida de taquicardia para compensar la hipoxia debida a la parálisis de los músculos respiratorios, fibrilación auricular o taquicardia ventricular y bloqueos aurículo-ventriculares.
Cianuro
La toxicidad por cianuro ocurre a menudo cuando se inhala humo, en la que se combinan el monóxido de carbono y el cianuro. El cianuro se une a la citocromo oxidasa celular y de este modo interfiere con la utilización aeróbica de oxígeno. Las alteraciones electrocardiográficas son similares a las que produce el monóxido de carbono.
Metales pesados
Las alteraciones electrocardiográficas producidas por la exposición al arsénico son la principal descripción de la intoxicación por metales pesados. La prolongación del QTc y la inversión de la onda T que produce este tóxico, puede persistir durante meses después de la recuperación clínica. En la intoxicación aguda por el arsénico es rara la presencia de Torsade de pointes y fibrilación ventricular.
REFERENCIAS
1. Reig-Valero R, Oltra-Chorda R. Electrocardiografía básica. En: Tejeda Adell. El paciente agudo grave. Barcelona (España). Masson 2005; 239-254 [ Links ]
2. Huszar RJ. Arritmias. Guía práctica para la interpretación y tratamiento. Tercera Edición. Madrid (España). Elsevier 2003
3. Levine HD, Wanzer SU, Merrill JP. Dialyzable currents of injury ín potassium intoxication resemblíng acute myocardial infarction or pericarditis. Circulation 1956; 13:29-36. [ Links ]
4. Commerford PJ, Lloyd E A. Arrhythmias in patients with drug toxicity, electrolyte, and endocrine disturbances. Med Clin North Am 1984; 68:1051-1078 [ Links ]
5. Daniel KR, Courtney DM, KHne JA. Assessment of cardiac stress from massive pulmonary embolism with 12-lead ECG. Chest2001; 120:474-481 [ Links ]
6. Valeriano J, Elson J. Electrocardiographic changes in central nervous system disease. Neurol Clin 1993;11:257-272 [ Links ]
7. Brouwers PJAM, Wijdicks EFM, Hasan D, et al. Serial electrocardiographic recording in aneurysmal subarachnoid hemorrhage. Stroke 1989; 20:1162-1167. [ Links ]
8. Connor RCR. Heart damage associated with intracranial lesions. BMJ 1968; 3:29-3146 [ Links ]
9. Kono T, Morita H, Kuroiwa T, et al. Left ventricular wall motion abnormalities in patients with subarachnoid hemorrhage: neurogenic stunned myocardium. J Am Coll Cardiol 1994; 24:636-640 [ Links ]
10. Dixit S, Castle M, Velu RP, et al. Cardiac involvement in patients with acute neurologic disease. Arch Intern Med 2000; 160.3153-3158 [ Links ]
11. Tokgo zoglu SL, Batur MK, Topc Uoglu MA, et al. Effects of Stroke localization on cardiac autonomic balance and sudden death. Stroke 1999; 30:1307-1311 [ Links ]
12. Chan TC, Vilke GM, Pollack M, et al. Electrocardiographic Lam HGT, Dekker W, Kan G, et al. Esophageal dysfunction as a cause of angina pectoris ("linked angina"): does it exist? Am J Med 1994; 96:359-364
13. Danzl DF, Pozos RS. Accidental hypothermia. N Engl J Med 1994; 331:1756-1760 [ Links ]
14. Van Mieghem C, Sabbe M, Knockaert. The Clinical Value of the ECG in Noncardiac Conditions. Chest 2004; 125:1561-1576 [ Links ]
15. Marius-Nunez AL. Myocardial infarction with normal coronary arteries after acute exposure to carbon monoxide. Chest 1990; 97: 491-494 [ Links ]
16. SaadehAM, Farskh NA, Al-Ali MK. Cardiac manifestations of acute carbamate and organophosphate poisoning. Heart 1997; 77: 461-464 [ Links ]


















