Introducción
La caries dental es una enfermedad crónica que afecta al 97% de la población mundial en las diferentes etapas de la vida, ocasiona la pérdida de las piezas dentarias, dificulta la masticación y puede ser el inicio de infecciones que afecten la pulpa dental (WHO, 2020; Mc Donald y Arevy, 1995). El agente etiológico más importante para el desarrollo de la caries es Streptococcus mutans, este microorganismo se transmite de una persona a otra mediante el beso y el compartir utensilios de alimentación (Barbería, 2001; Fejerskov, 2006: Alaluusua y Renkonen, 2004).
Los primeros estudios que demostraron el papel que desempeñan los microorganismos en el desarrollo de caries dental fueron: Miller en el año 1882, elaboró la teoría quimioparasitaria que se fundamenta en la capacidad de un gran número de bacterias bucales, de producir ácidos a partir de los hidratos de carbono de la dieta (Kidd y Fejerskov, 2016; Liebana Ureña, 2002), hipótesis que posteriormente se sustentó con el aislamiento de microorganismos cariogénicos. Las primeras pruebas experimentales se realizaron en el año 1946 (McClure y Hewitt, 1946) demostraron que la penicilina inhibía la caries en ratas y Orland et al (1945) demostraron que las ratas libres de gérmenes no desarrollaban caries aun teniendo una dieta rica en carbohidratos fermentables, cuando se infectó a estas ratas con microorganismos capaces de fermentar los hidratos de carbono produciendo ácidos aparecieron las lesiones cariosas. Keyes (1960) demostró que en hamsters con caries activa tenían placa bacteriana con gérmenes específicos concretamente estreptococos a diferencia de los hamsters sin caries presentaron ausencia de los mencionados gérmenes en placa bacteriana, comprobando la transmisibilidad de los microorganismos cariogénicos en placa dental de unos hamsters a otros infectándolos. Posteriormente Fitzgerald y Keyes (1960) demostraron definitivamente la cariogenicidad de los estreptococos y Fitzgerald et al (1980) demostraron la implicación de los Lactobacillus.
Actualmente se valida la teoría de Miller para indicar que la caries se debe a la presencia de una placa dental cariogénica capaz de reducir el pH hasta niveles en los que se produce la desmineralización de los tejidos duros del diente (Thylstrup y Fejerskov, 1988). Según Fejerskov (2004), la caries tiene un origen multifactorial involucrando factores biológicos, socio económicos y culturales del ser humano que actúan directa o indirectamente en el establecimiento de S. mutans y otros microorganismos cariogénicos, capaces de formar una placa bacteriana dental cariogénica. Según Keyes (1960), para el desarrollo de la caries, el paciente debe presentar elevados niveles de S. mutans y Lactobacillus, consumir frecuentemente alimentos dulces principalmente sacarosa refinada y disminución en la frecuencia del cepillado dental.
La placa bacteriana es más cariogénica cuando las bacterias que la componen tienen una elevada capacidad de adherencia a la placa, las bacterias que son capaces de sintetizar polisacáridos extracelulares del tipo glucanos y levanos, compuestos muy viscosos, son S. mutans y Lactobacillus (Leite et al, 2020). La propiedad de acidogenicidad que posee principalmente S. mutans es la capacidad de producir ácidos a partir de los hidratos de carbono de la dieta para liberar al medio ácido láctico, compuesto que desmineraliza los tejidos duros del diente y ocasiona caries, pero también la tienen los Actinomyces, Bacteroides, Fusobacterias y Nocardia entre otros (Mundorff et al, 2000; Kidd y Fereskov, 2004). La alta acidofilia, que es la facultad de adaptarse y tolerar bien el medio ácido, siendo los Lactobacillus (pH<5) y los S. mutans (pH <5,2) los que mejor sobreviven en medios con pH bajo (Newbrum, 2004), además S. mutans tiene la capacidad de sintetizar y utilizar polisacáridos intracelulares de reserva para producir ácido en ausencia de sustrato de la dieta (Kidd y Fereskov, 2016; Fitzgerald et al, 1980). Por el contrario, microorganismos que podrían estar presentes como bacterias comensales, son capaces de utilizar ácidos para su metabolismo, cono es el caso de Veillonella alcalescens, que consume ácido láctico, o bacterias que producen sustancias alcalinas que aumentan el pH de la placa como hacen los bacilos Gramnegativos, entonces la placa dental será no cariogénica (Grindefjord et al, 2005).
En la actualidad se cuentan con varios métodos de identificación de actividad de caries como: el recuento de S. mutans en placa bacteriana y saliva, determinación del pH salival para valorar la capacidad tampón y la detección de placa cariogénica con la medición de pH antes y después de la administración de una solución de sacarosa al 10% (Grindefjord et al, 2005; Caufield et al, 2003), estás dos últimas técnicas son económicas y de fácil aplicación. Es así que en la presente investigación se pretende determinar la actividad de caries mediante el descenso del pH de la saliva y placa bacteriana, evaluando indirectamente la capacidad de los microorganismos cariogénicos de metabolizar la sacarosa y transformar en ácidos.
Material y Métodos
Enfoque y tipo de investigación
Lainvestigaciónpresentaunenfoquecuantitativo, cuasiexperimental de ensayo clínico controlado, los investigadores administran a los pacientes sacarosa al 10% para valorar la actividad de riesgo de caries, evaluando indirectamente el metabolismo de microorganismos cariogénicos principalmente S. mutans, que transforman la sacarosa en ácido láctico produciendo el descenso del pH en la placa bacteriana dental y de la saliva.
Población de estudio
Participaron en el estudio 33 niños comprendidos entre las edades de 6 a 12 años, quienes fueron atendidos en la clínica de Odontopediatría de la Facultad de Odontología, para formar parte del estudio los participantes cumplieron con los siguientes criterios de inclusión y exclusión: Fueron excluidos los niños que se encontraban con medicación antibiótica o antiséptica en el momento del estudio y fueron incluidos los niños que no cepillaron las piezas dentales por lo menos una hora antes de la toma de muestra.
Se confeccionó una ficha de registros de datos como: edad, sexo, consumo de sacarosa, índice de placa y de caries, pH de la saliva y actividad de placa cariogénica.
Determinación de índice de caries por el método de Klunes
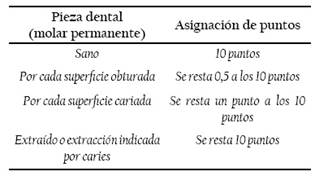
El índice de caries se realizó observando los cuatro primeros molares permanentes, asignándoles un puntaje a cada condición con un máximo de 10 puntos por cada molar.
Tabla 1. Determinación de índice de caries por el método de Klunes
Determinación de índice de placa bacteriana según IHOS
Se determinó el grado de higiene oral examinando las piezas dentales N° 16 (1º molar superior derecho permanente); N° 26 (1º molar superior izquierdo permanente) ubicadas en el maxilar superior y las piezas dentales: N° 36 (1º molar inferior izquierdo permanente); N° 46 (1º molar inferior derecho permanente) del maxilar inferior (Mc Donald y Avery, 1995; Barberia, 2001).
Para valorar la placa bacteriana de las superficies dentales, se consideró en el análisis todas las superficies de dichos dientes, con un valor máximo de 6 y un valor mínimo de 0 contabilizando detritos y cálculo (Mc Donald y Avery, 1995; Alaluusua y Renkonen, 2004).
Fig.1. Determinación de los Índices de caries y placa bacteriana dental
Determinación de pH en la saliva del paciente
Para la determinación del pH se pidió al paciente que acumule saliva en la base de la boca y con la ayuda de una pipeta Pasteur de plástico se recolectó la saliva en una cantidad aproximada de 3 ml y se vació en un tubo de ensayo estéril, la muestra se colectó antes y después de la administración de la solución de sacarosa al 10%. para luego determinar el pH con un peachímetro de marca Extech. El pH de la saliva en condiciones normales es de 6,5 a 7,5, pH menor a 5,2 indica riesgo de caries (Thylstrup y Fejerskov, 1998; Newbrum, 2004).
Determinación de placa bacteriana cariogénica
Para determinar placa bacteriana cariogénica se tomó muestra de placa bacteriana de las piezas dentales en las zonas inter proximales y cerca del margen gingival, la muestra se depositó en un tubo de ensayo, luego se administró una solución de sacarosa al 10% por vía oral, para que el paciente retenga en su boca por el tiempo de 1 min, cumplido el tiempo el paciente escupió la solución. Después de 10 minutos se volvió a tomar muestra de placa bacteriana repitiendo el procedimiento anterior, para luego determinar el pH con el peachímetro portátil.
Finalmente se compararon los valores de pH de las muestras tomadas antes y después de la administración de la solución de sacarosa. Si se observó descenso del pH se concluyó que el paciente presentaba riesgo de caries (Fitzgerald et al, 1980; Leite et al, 2020; Mundorff, 2000).
Fig.2 Toma de muestra de saliva y placa bacteriana dental para la determinación de Ph
Fig.3 Determinación del pH de la saliva y placa bacteriana dental antes y después de la administración de sacarosa
Resultados
Participaron en el estudio 33 niños atendidos en la clínica de Odontopediatría las edades fueron de 6 a 12 años, se registró la edad, sexo, índices de placa y de caries, así como el pH de la saliva y la actividad de placa cariogénica.
La distribución según sexo fue de 20 varones y 13 mujeres. Una de las variables que se determinó en el estudio fue el consumo de sacarosa preguntando la frecuencia de consumo de dulces, galletas y gaseosas. El consumo de sacarosa en la mayoría de los niños fue entre 3 a 5 veces por semana y muestra relación con el índice de caries mayor a 75% (Tabla 2).
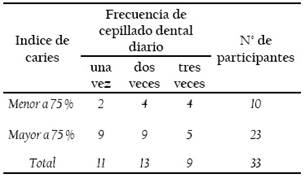
El 75,48% de la población estudiada presentó caries dental con índices que oscilaron entre 22,0 % al 95,50%. Respecto a la frecuencia del cepillado 11 niños se cepillan los dientes una vez al día, 13 dos veces al día y 9 tres veces al día (Tabla 3).
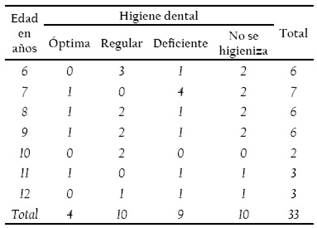
En cuanto al índice de placa 29 participantes presentaron elevados índices de placa mayor a 4, es decir con higiene regular a deficiente o no se higienizan las piezas detales. Los niños menores de 9 años presentaron una higiene dental deficiente (Tabla 4).
Mediante la técnica de determinación de riesgo cariogénico de placa bacteriana, suministrando sacarosa al 10% en pacientes pediátricos se expone que la técnica fue un buen indicador de riesgo de caries, según los datos estadísticos de la prueba de t de student para muestras relacionadas, la sacarosa es un buen sustrato para el metabolismo de microorganismos cariogénicos (S. mutans), por la rápida transformación de este azúcar en ácidos.
Los valores de la significación bilateral fueron menores a 0,0001 con un 95% de confianza, es decir se observa una significativa diferencia estadística entre las medias del pH antes y después de la administración de la sacarosa en los participantes (Tabla 5).
En el estudio también se determinó el pH de saliva antes y después de la administración de sacarosa al 10%. Antes de la administración de sacarosa el pH de saliva de 2 niños fue alcalino (> 8); 26 niños presentaron un pH comprendido entre 6,5 y 7,5; 4 niños destacaron pH ácido (< 5).
Después de la administración de la solución de sacarosa 21 niños presentaron pH ácido y 12 destacaron pH neutro a ligeramente alcalino.
Con la aplicación de la prueba t student para muestras relacionadas, los valores de la significación bilateral fueron menores a 0,0001 con un 95% de confianza, es decir se observó una significativa diferencia estadística entre las medias del pH antes y después de la administración de la sacarosa en los participantes (Tabla 6).
Discusión
En la cavidad bucal se dan condiciones micro ambientales ideales de temperatura y aporte de nutrientes adecuados para el desarrollo de un amplio rango de microorganismos en su mayoría comensales que se adhieren a la superficie dentaria a través de una película adquirida acelular para formar la placa bacteriana (Mundorff. 2000). Si la persona no realiza el control químico y mecánico de esta placa para removerla constantemente, se formará el tártaro o cálculo dental que es precursor para el desarrollo de enfermedades buco dentales prevalentes en el país como la caries y los procesos periodontales como la gingivitis y periodontitis (; Poyato et al, 2001; Caufield et al, 2003).
La sacarosa es el edulcorante natural más utilizado y el principal sustrato relacionado con la frecuencia de caries dental en la población infantil (Habibian et al, 2002), en el estudio se detectó elevado consumo de sacarosa refinada por los participantes, se observó que, a mayor frecuencia de consumo de galletas, gaseosas y dulces, mayores fueron los índices de caries. Se conoce que la sacarosa es fácilmente metabolizada por las bacterias de la cavidad bucal, las que se encuentran en la placa dental principalmente S. muntans que presenta la propiedad acidogénica, capacidad de transformar los azúcares en ácidos, responsables de la desmineralización de los tejidos duros del diente esta dinámica ocasiona la caries dental (Berkowitz et al, 2008).
Mediante el método de Klunes, se detectó que el índice de caries en la población estudiada fue de 75,48%, este valor superior es frecuente en nuestro medio por el alto consumo de azúcares y las deficiencias en la higiene dental, contextos similares a Bolivia como, México, Ecuador y Perú reportan índices de caries en poblaciones infantiles de 6 a 12 años de 78%, 62,39% y 85,43% respectivamente , según las conclusiones de las sociedades de Odontopediatría de los países de Latinoamérica especifican que es importante elaborar, ejecutar, implementar y vigilar los programas preventivos de salud oral, especialmente en grupos con vulnerabilidad social (Martins, 2014).
En cuanto al índice de placa bacteriana por el método de la IHOS se detectó en los pacientes que participaron en el estudio presentaron niveles altos de índice de placa mostrando una higiene regular a deficiente, caso que promueve la fácil colonización y producción de ácidos por microorganismos cariogénicos principalmente S. mutans para el desarrollo de caries dental (Lamas et al, 2005; Horowitz, 2010; Fejerskov et al, 2015).
Se conoce que la cariogenicidad de la placa dental depende de la presencia de bacterias capaces de reducir el pH hasta niveles de producir desmineralización de los tejidos duros del diente (Fejerskov. 2006; Alaluusua y Renkonen, 2004; Kidd y Fejerskov, 2016). El pH de la placa bacteriana en ayunas normalmente es neutro o ligeramente ácidos en personas con baja actividad de caries, pero disminuye rápidamente tras la exposición a azúcares y luego se va elevando hasta alcanzar el valor inicial o de reposo en 30 a 60 minutos (Liebana Ureña, 2002).
En nuestro estudio el pH de la placa dental de 30 niños antes de administrar la solución de sacarosa al 10% fue igual o inferior a 6,5 y solo 3 niños destacaron un pH igual o superior a 7,0. Con la ingesta de azúcares refinados el pH de la placa bacteriana dental alcanza un punto crítico entre 5,2 y 5,5 para la producción de la caries dental (Leite et al, 2020; Mundorff et al, 2000).
La desmineralización del esmalte sólo se produce cuando los ácidos bacterianos (responsables de la caída de pH disuelven la hidroxiapatita aun pH igual o inferior a 5,0, este pH tan bajo es consecuencia de la producción de ácido láctico en un 50%, ácido acético y fórmico, estos ácidos son liberados por las bacterias al fermentar los hidratos de carbono de la dieta (Leite et al, 2000; Kidd y Fejerskov, 2004; Newbrum, 2004; Kidd y Fejerskov, 2013; Fejerskov y Bente, 2017; Park et al, 2022).
Respecto al pH de la saliva que en condiciones normales es de 6,5 a 7,5 la mayor parte de los participantes presentaron niveles menores a 6,5 antes y después de la administración de la solución de sacarosa al 10%, entonces es un buen indicador de riesgo de caries (Viana et al, 2021).
Finalmente, con estas pruebas sencillas se logró determinar el riesgo de caries de la población infantil, evaluando indirectamente la capacidad metabólica de los microorganismos cariogénicos.