Journal of the Selva Andina Animal Science
versión impresa ISSN 2311-2581
J.Selva Andina Anim. Sci. vol.7 no.2 La Paz 2020
https://doi.org/10.36610/j.jsaas.2020.070200050
Artículo de Investigación
Parámetros morfométricos del espermatozoide de alpaca (Vicugna pacos), obtenidos por tres métodos de colección
Morphometric parameters of alpaca spermatozoa (Vicugna pacos), obtained by three collection methods
Huanca-Marca Nancy Frinee1*![]() , Ordoñez-Rodríguez Cesar Domingo1, Quispe-Ccasa Hurley Abel2
, Ordoñez-Rodríguez Cesar Domingo1, Quispe-Ccasa Hurley Abel2![]() , Antezana-Julian Walter Orestes1
, Antezana-Julian Walter Orestes1![]() , Jordan-Misme Luis Alipio1
, Jordan-Misme Luis Alipio1![]() , Ampuero-Casquino Enrique1
, Ampuero-Casquino Enrique1![]() , Cucho-Dolmos Hernán Carlos1
, Cucho-Dolmos Hernán Carlos1![]()
1Departamento Académico de Ganadería. Escuela Profesional de Zootecnia. Facultad de Ciencias Agrarias. Universidad Nacional de San Antonio Abad de Cusco. Granja Kayra S/N, San Jerónimo, Cusco, Perú. Av. de La Cultura 773, Cusco 08000, Perú Telf. +51.84.604100 - 51.84.604160 Fax 51.84.238156 AP 921 - Cusco, Perú
2Escuela de posgrado. Universidad Nacional Toribio Rodríguez de Mendoza de Amazonas. Campus Universitario: C. Higos Urco N° 342-350-356. Chachapoyas 01001, Perú. Tel: 041-477694 / DGAYRA: 041-478821
*Dirección de contacto: Departamento Académico de Ganadería. Escuela Profesional de Zootecnia. Facultad de Ciencias Agrarias. Universidad Nacional de San Antonio Abad de Cusco. Granja Kayra S/N, San Jerónimo, Cusco. Av. de La Cultura 773, Cusco 08000, Perú. Telf. +51.84.604100 - 51.84.604160 Fax 51.84.238156 AP 921 - Cusco, Perú.
Nancy Frinee Huanca-Marca
E-mail address: frineehm92@gmail.com
Historial del artículo.
Recibido junio 2020.
Devuelto agosto 2020.
Aceptado septiembre 2020.
Disponible en línea, octubre 2020.
ID del artículo: 075/JSAAS/2020
J. Selva Andina Anim. Sci. 2020; 7(2):50-62.
Resumen
La morfología espermática es esencial en la evaluación de la calidad seminal e importante para la predicción de la fertilidad de machos reproductores. El objetivo del presente estudio fue comparar los parámetros morfométricos de espermatozoides de alpaca, obtenidos por tres métodos de extracción de semen, la recuperación del conducto deferente (DCD), electroeyaculación (EE) y aspiración vaginal (AV). La colección se realizó de 3 animales por cada método. Se determinó la movilidad, concentración, vitalidad, funcionalidad de membrana y parámetros de morfometría espermática, con un equipo de análisis computarizado de semen - ISAS® CASA - Morph. Para los parámetros morfométricos, las muestras de semen se procesaron con un kit de tinción Hemacolor® y se observaron en un microscopio de contraste de fases. Por cada muestra, se capturaron al menos 200 espermatozoides al azar, con resolución de imágenes de 0.08 μm por píxel en los ejes horizontal y vertical. La motilidad total fue de 16.27±11.96%, 14.68±11.21% y 12.44±7.27%, la concentración espermática de 247±186.70 x 106EPZ/mL, 67.92±67.92 x 106EPZ/mL y 100.32±56.13 x 106EPZ/mL, la vitalidad fue 62.86±15.92%, 63±15.21% y 70.16±14.33% en espermatozoides colectados por DCD, EE y AV respectivamente. En cuanto a los parámetros morfométricos se encontró una longitud de 5.49±0.43 µm, 5.53±0.41µm y 5.75±0.53µm, área 14.30±2.0µm2, 15.05±1.77µm2 y 15.88±2.0µm2, perímetro de 16.10±1.31µm, 17.11±1.20µm y 17.41±1.43µm, ancho de 3.22±0.27µm, 3.30±0.32µm y 3.33±0.25 µm y el porcentaje de acrosoma de 52.22±7.82%, 49.52±7.47% y 47.44±5.77% en espermatozoides colectados por DCD, EE y AV respectivamente. La comparación de los parámetros morfométricos entre método de colecta y animal se realizó mediante un diseño de bloques alzar. Los parámetros morfométricos del tamaño y forma de la cabeza de espermatozoide, y pieza intermedia mostraron diferencias estadísticas significativas (p<0.01) entre métodos de colección y entre animal. En conclusión, los parámetros morfométricos del espermatozoide de alpaca son influidos por el método de colección, y muestran variación entre animales.
Palabras clave: Alpaca, método colecta, espermatozoide, morfometría, CASA, ISAS®
Abstract
Sperm morphology is essential in evaluating seminal quality and important for fertility prediction in breeding males. The aim of this study was to compare the morphometric parameters of alpaca sperm, collected using three methods of semen extraction, recovery of the vas deferens (DCD), electro ejaculation (EE) and vaginal aspiration (VA). The collection was made of 3 animals by each method. The mobility, concentration, vitality, membrane functionality and sperm morphometry parameters were determined in a computerized semen analysis kit – ISAS® CASA - Morph. For morphometric parameters, semen samples were processed with a Hemacolor® staining kit and viewed under a phase-contrast microscope. For each sample, at least 200 sperm were captured at random, with an image resolution of 0.08 µm per pixel on the horizontal and vertical axes. The comparison of the morphometric parameters between the collection method and the animal was carried out using a random block design. Total motility was 16.27±11.96%, 14.68±11.21% and 12.44±7.27%; the sperm concentration of 247±186.70x106EPZ/mL, 67.92±67.92x106EPZ/mL and 100.32±56.13x106EPZ/mL, the vitality was 62.86 ±15.92%, 63±15.21% and 70.16±14.33% in sperm collected by DCD, EE and AV respectively. Regarding the morphometric parameters, a length of 5.49±0.43µm, 5.53±0.41µm and 5.75±0.53µm was found, area 14.30±2.00 µm2, 15.05±1.77 µm2 and 15.88±2.00 µm2, perimeter of 16.10±1.31µm, 17.11±1.20µm and 17.41 ± 1.43, width of 3.22±0.27µm, 3.30±0.32µm and 3.33±0.25µm and the acrosome percentage of 52.22±7.82µm, 49.52±7.47µm and 47.44±5.77µm in sperm collected by DCD, EE and AV respectively. The morphometric parameters of the size and shape of the sperm head and the intermediate piece showed significant statistical differences (p <0.01) between the collection methods and between the animals. In conclusion, the morphometric parameters of alpaca spermatozoa were influenced by collection method, and show variations between animals.
Keywords: Alpaca, collection method, spermatozoa, morphometry, CASA, ISAS®
Introducción
La colección de semen en camélidos sudamericanos (CSA) presenta inconvenientes como la duración, posición de la cópula, alta viscosidad, bajo volumen de los eyaculados, así como baja concentración espermática, ausencia de movilidad progresiva, difícil manejo, motivando la búsqueda de una técnica óptima para extraer semen y poder manipular los espermatozoides (EPZ), sin que estos pierdan su capacidad fecundante1,2. La colección de semen depende de una buena y constante producción espermática para su calidad, las técnicas de colección están muy desarrolladas en otras especies domésticas, en las cuales ya existe un procedimiento de rutina, pero en CSA no hay un protocolo recomendado y una técnica optima, por ende, las características seminales son muy variables y dependen de la forma de colección y existen varios factores que afectan su calidad3.
De todos los parámetros de calidad seminal analizados en un eyaculado, tales como volumen, concentración, movilidad, vitalidad y morfología espermática, se reconoce que la morfología es una característica determinante, para diagnosticar problemas de fertilidad de machos y predecirla en trabajos de inseminación artificial (IA)4,5. La utilización de valores de referencia morfométricos de los EPZ puede aumentar el conocimiento de su capacidad para la fertilización natural e in vitro, así como su calidad y función después de la criopreservación6 la evaluación morfológica y morfométrica de la estructura del acrosoma de los EPZ permite la predicción precisa de la capacidad de fertilización de los machos7,8. En este contexto la determinación de la estructura morfológica de estos es de particular importancia, porque su tamaño y forma son criterios importantes en la clasificación de los EPZ como normales y anormales. No solo el tamaño de la cabeza afecta la capacidad de fertilización, sino también las dimensiones y función de la cola y pieza central9.
En los CSA el 40% de EPZ de un eyaculado tiene una morfología normal10, es por ello se viene realizando varios estudios, debido a que la forma, tamaño de la cabeza, del núcleo espermático, están relacionados con el contenido de ADN y la organización de la cromatina11, es fundamental analizar la morfología espermática de reproductores, porque las anormalidades del núcleo están frecuentemente asociadas con una reducción de fertilidad12.
Sin embargo, la caracterización, clasificación precisa de la morfología espermática, requiere técnicas objetivas de medición y métodos estandarizados de tinción. Por ello, el uso de sistemas de análisis espermático asistido por computadora (CASA) de muestras de semen teñidas, ha significado un avance en el análisis preciso de la morfología espermática, en base a una serie de parámetros13,14. En CSA, los estudios sobre morfología y morfometría de EPZ de llama y alpaca son escasos11,15-21 donde se utilizaron diferentes protocolos de tinción con Hemacolor®, Diff Quick®, Papanicolaou y Tinción 15®.
En ese sentido, el presente estudio tuvo como objetivo comparar los parámetros morfométricos del EPZ de alpaca (Vicugna pacos) entre tres métodos de extracción de semen, desviación de conducto deferente, electroeyaculación y aspiración vaginal.
Materiales y métodos
Lugar y animales del estudio. El estudio fue realizado en el Centro de Investigación en Camélidos Sudamericanos (CICAS) La Raya, de la Facultad de Ciencias Agrarias (FCA) de la Universidad Nacional de San Antonio Abad del Cusco (UNSAAC), ubicado a 4133 metros de altitud, de enero a junio del 2017. El grupo experimental estuvo conformado por 9 alpacas macho adultos de 6 a 8 años de edad y peso promedio de 69.11±9.84 kg, mantenidas en una pradera natural conformada por asociaciones de gramíneas (festucas, stipas y calamagrostis) y agua a libre acceso.
Colección de semen. La extracción de semen se realizó por tres métodos: recuperación de EPZ por desviación del conducto deferente (DCD), electroeyaculación (EE) y aspiración vaginal (AV), asignando 3 alpacas por cada método. Para la recuperación de EPZ por DCD se utilizaron alpacas previamente intervenidas quirúrgicamente y desviados los conductos deferentes hacia la cara interna del muslo21 Por medio de una fistula, las gotas de EPZ fueron succionadas y depositadas en tubos viales de 2 mL22, que contenían 0.3 mL de dilutor base Tris, fructosa y ácido cítrico, a 37 °C23. Para la extracción de semen por EE se tomó como referencia el protocolo de Director et al.24 con modificaciones para alpacas, bajo anestesia general (Ketamina 2.5 mL/100 kg PV y Xylazina 0.2 mL/20 kg PV por vía intravenosa)25, se aplicó ciclos crecientes de 2 a 12 V, con alternancia de periodos de estimulación eléctrica de tres segundos y con intervalos de reposo de un segundo con el electroeyaculador (ElectroJac 5®, Ideal Instruments®, Lansing, EU). Las muestras de semen por AV fueron extraídas de hembras luego de un periodo de cópula de 20 a 40 min con machos seleccionados, introduciendo un espéculo vaginal hasta el cérvix, realizando movimientos giratorios y verticales en el mismo eje26 En todos los casos, las muestras fueron inmediatamente conservadas a 37 °C.
Evaluación microscópica. La movilidad total (móviles progresivos y móviles no progresivos) y la concentración de EPZ se evaluaron en el equipo ISAS®, Integrated Semen Analysis System (Proiser R+D, Paterna, Valencia, España), equipado con un microscopio de contraste de fases UOP - UB200i, objetivo 10x de contraste de fase negativo, con una video cámara (Ximea MQ003MG-CM, Ximea, Münster, Alemania). La vitalidad se determinó mediante fluorescencia, usando el kit VitalTest® (Halotech, Madrid, España) (solución de naranja de acridina y solución de yoduro de propidio), siguiendo las especificaciones del fabricante. Para evaluar la funcionalidad de la membrana espermática se empleó una solución hipoosmótica de 50 mOsm/kg27, donde la adecuada función de membrana se evidencio con reacción positiva al enrollamiento de la cola (HOST+). Para determinar los porcentajes de vitalidad y HOST+ se contabilizaron no menos de 200 EPZ, con el objetivo de 40X del ISAS®.
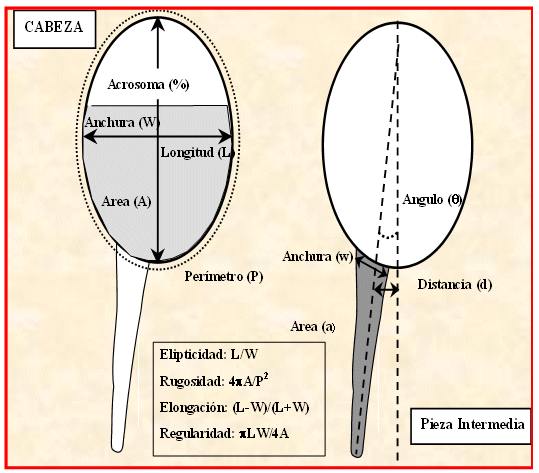
Morfometría espermática. Los portaobjetos con muestras de semen fueron secados al ambiente y sometidos al protocolo de tinción del kit Hemacolor® (Merck, Darmstadt, Alemania), siguiendo las recomendaciones del fabricante. El análisis morfométrico de las muestras se realizó en el módulo de morfometría del ISAS®, con el objetivo de 100X y aceite de inmersión. El tamaño del marco de captura de fotogramas de video fue de 768x576x8 bits y 256 niveles de gris. La resolución de las imágenes fue de 0.08 μm por píxel en los ejes horizontal y vertical. Se capturaron al azar no menos de 200 EPZ por muestra, sin presentar superposiciones entre EPZ. Se analizaron 13 parámetros morfométricos, del tamaño de cabeza del EPZ (figura 1) fueron longitud (L, µm), ancho (W, µm), área (A, µm2) y perímetro (P, µm), de los que derivan los parámetros de forma, como elipticidad (L/W), elongación ([LW]/[L+W]), regularidad (πLW/4A) y rugosidad (4πA/P2). Además, del porcentaje de acrosoma (% del total de la cabeza), ancho y el área de la pieza intermedia (PI) en µ, distancia de inserción de PI (entre la cabeza y el eje de la PI, µm) y el ángulo de inserción de PI5,22 por los tres métodos de colección (figura 2).
Figura 1 Parametros morfometricos estudiados en este estudios segun Soler et al.5
Análisis estadístico. Se obtuvo la estadística descriptiva de la movilidad, concentración, vitalidad y funcionalidad de la membrana espermática. Se determinaron los supuestos de normalidad y homocedasticidad mediante las pruebas de Kolmogorov-Smirnov y Levene para los datos obtenidos del análisis CASA-Morph de todas las células analizadas. Para los datos que no tenían una distribución normal se realizó su transformación con el procedimiento TRANSREG del SAS. La comparación entre métodos de colecta de semen se efectuó bajo un diseño de bloques al azar, la comparación de medias se realizó con el test de Duncan. Para los cálculos estadísticos se utilizó el SAS v. 8.2 (North Carolina State University- United States)
Yijk = µ + Ai + Cj+ eijk.
Donde:
Yijk = Variable respuesta.
µ = Media poblacional o constante común.
Ai = Efecto animal
Cj = Efecto del tipo de colección
eijk= Error Experimental.
Resultados
|
|
| * Letras distintas en la fila indican diferencias altamente significativas (p ≤ 0,01) *Prom: promedio, DS.: Desviación estándar; PI: Pieza intermedia |
|
|
| *Letras distintas en la columna indican diferencias altamente significativas (p ≤ 0.01). DS.: Desviación estándar |
Discusión
La determinación de características microscópicas rutinarias, de EPZ de alpacas obtenidas por tres métodos de colección: movilidad total (MT), concentración espermática (CE), vitalidad y funcionalidad de membrana espermática (FMP), se observan en la tabla 1. Estos hallazgos están dentro de los rangos descritos por Meza et al.21y Quispe28 en EPZ recuperados del conducto deferente, Alarcón et al.29 en semen colectado por AV, y de Flores et al.25, Ordoñez et al.30 y Ciprian31 en semen colectado por EE, todos ellos en alpacas. Todas las variables microscópicas se evaluaron en 9 colecta por cada método de extracción de semen.
|
|
Los valores de los parámetros morfométricos del tamaño de la cabeza de EPZ (longitud, ancho, área y perímetro), forma de la cabeza (elipticidad, rugosidad elongación y regularidad), porcentaje de acrosoma, ancho, área, distancia y ángulo de inserción de la pieza intermedia de los EPZ, tabla 2. El método de colecta influyó significativamente en todos los parámetros morfométricos de tamaño de la cabeza del EPZ (p<0.01) (tabla 2). Las dimensiones morfométricas de tamaño de cabeza de EPZ obtenidos por DCD fueron menores que por EE y AV. Esta gran variabilidad morfométrica entre métodos de colecta, probablemente se deba a la presencia de plasma seminal (EE) y fluidos del tracto de la hembra (AV), ya que los EPZ recuperados del conducto deferente están desprovistos de las secreciones de la próstata y glándulas bulbouretrales, que conforman un eyaculado completo. Por lo tanto, la mayoría de EPZ colectados por DCD probablemente no hayan completado su maduración. El plasma seminal juega un rol importante en la conservación de los EPZ, porque contiene antioxidantes como vitamina C, vitamina E, urato, albumina, taurina, hipotaurina, piruvato y lactato, además de proteína secretora rica en cisteína (CRISP3), asociada positivamente con la tasa de concepción32,33.
Algunos parámetros son similares a los reportes de Buendía et al.15 Casaretto et al.34, Ordoñez et al.16, Soler et al.35 Giuliano & Ferrari36, Evangelista-Vargas et al.18 Flores-Huarco37 y Cucho et al.22 Por ejemplo, Ordoñez et al.16 refieren dimensiones de tamaño de cabeza más grandes (largo 5.89 μm, ancho 3.50 μm y perímetro 17.53 μm) en semen de AV, coloreado con Diff Quick® y evaluado en ISAS® lo cual probablemente se deba al tipo de tinción utilizada, por su parte Buendía et al.15 señalan mayor longitud y ancho de cabeza (6.10 μm y 3.62 μm, respectivamente) y menor perímetro (15.11 μm), en semen de alpaca colectado por AV, coloreado con Hemacolor® y evaluado en SCA®. Para comprender estas diferencias, se podría hipotetizar que en el semen completo (EE), la presencia de plasma seminal, o células sanguíneas, mucosidad vaginal y otras impurezas (AV), podrían estimular la reacción acrosomal. Ordoñez et al.16 reportaron menor porcentaje de acrosoma respecto a la cabeza (46.58%) colectados por AV, Ciprian33 (49.95% y 56.08%) en EPZ colectados por EE y DCD. El acrosoma es una estructura directamente relacionada con la fertilidad38. Cada EPZ está dotado de un único acrosoma, cuya forma y tamaño varía ampliamente entre las especies39. La reacción acrosomal inducida natural o artificialmente depende de la tinción utilizada puede generar la pérdida de la misma o sobrestimación del tamaño de la cabeza del EPZ40. Aunque Yániz et al.14 sugiere emplear técnicas de fluorescencia para diferenciar estructura de los EPZ. Cucho et al.22 considera que la tinción adecuada para EPZ del conducto deferente es Hemacolor®, porque permite determinar la presencia y proporción del acrosoma en la cabeza espermática.
De igual forma, se encontró diferencias estadísticas significativas en los parámetros de forma de cabeza, y de la pieza intermedia (PI) de los EPZ (p<0.01) (tabla 2). Desde un punto de vista patológico, se sostiene que las condiciones ambientales adversas como alta temperatura y humedad, podrían generar hidrocele y edema escrotal en los animales, alterando las características macroscópicas y microscópicas de los eyaculados y en los parámetros morfométricos de los EPZ41. Sin embargo, en virtud de la diversidad morfológica de los EPZ de alpaca, se atribuyen diversas aptitudes funcionales de acuerdo a las características morfológicas de los EPZ. Así, Núñez-Martínez et al.42 afirman que existe una variable criopreservabilidad entre subpoblaciones, la cual depende de la gradiente osmótica según forma, volumen y área celular (parámetros usados para estimar rugosidad y regularidad).
Existen escasos reportes del estudio de la morfometría de la PI espermática, Cucho et al.22 halló valores similares con Hemacolor®, pero Ordoñez et al.16 obtuvieron mayores valores, en EPZ colectados por (AV) y con tipo de tinción empleado (Diff Quick®). La tinción influye en las dimensiones morfométricas reales de los EPZ, donde el esperma sufre deformaciones ya sea por ósmosis o deshidratación los EPZ pueden reducirse hasta 20% de la longitud y 13% de ancho de cabeza, estas características son necesarios para efectuar el análisis en sistemas CASA43. Cucho el al.22 indica que los resultados de la morfometría de esperma de alpaca son sensibles a la técnica de tinción aplicada. Lüpold et al.44 hallaron asociación entre la longitud de la PI y la motilidad espermática, ya que una mayor motilidad estaría relacionada a una mayor cantidad de energía producida en más mitocondrias presentes en una PI más elongada45. Sin embargo, Malo et al.46 sostiene que una PI más grande puede dificultar la locomoción de los EPZ, haciéndolos más lentos. La alta variabilidad en el ángulo de inserción de la PI (tabla 2) puede deberse a la acción mecánica de la extensión (frotis) y secado, influyendo en su cálculo.
Los parámetros morfométricos del tamaño de la cabeza de EPZ como longitud, ancho, área, perímetro y porcentaje de acrosoma de cada animal se observa en la (tabla 3). Donde las variables de los parámetros morfométricos (longitud, ancho, área, perímetro y porcentaje de acrosoma) tienen una variación individual en las alpacas (p<0.01).
La alta variación de dimensiones espermáticas entre individuos y dentro del eyaculado de un mismo individuo (tabla 3), podría apoyar la hipótesis de heteromorficidad espermática de camélidos por el alto grado de polimorfismos en un mismo eyaculado47. Las variables microscópicas del semen en camélidos sudamericanos varían entre individuo y además estas se ven afectadas tanto por el método de recolección como por la estación48. La morfología espermática en diferentes especies es variable entre individuos de la misma especie, raza, entre eyaculados del mismo individuo e incluso como subpoblaciones morfométricas dentro de un mismo eyaculado, debido al estado fisiológico, madurez sexual y polimorfia genética que controla la espermatogénesis46,49,50.
La importancia del papel de la morfometría de los EPZ en los últimos años ha tomado mucha importancia en todas las especies; por ejemplo, Maree et al.51 menciona la relación entre la morfometría del esperma y la fertilidad en humanos, y existen estudios que indican la relación entre las dimensiones del EPZ y la fertilidad en caballos52-55 en la que los trastornos de fertilidad se correlacionan positivamente con el tamaño de las cabezas espermáticas. La relación entre la morfología de los EPZ y la fertilidad también se ha estudiado en verracos56, toros57,58, perros59 y zorros60. Las principales fuentes de variación en la morfometría de los EPZ es la preparación de la muestra, método de fijación, sistema microscópico, actividad del técnico y método de colecta, todo esto puede afectar la repetibilidad del análisis, su reproducibilidad y la comparación de los resultados entre laboratorios61.
Es de gran importancia que el método de colecta sea ideal para la colección de EPZ y este no afecte a la morfología, en la estructura y en el tamaño de los EPZ.
Los resultados indican que la elección del método de colección de semen tiene un impacto en las dimensiones de la cabeza de los EPZ y en los parámetros morfométricos; en la que los EPZ recuperados por DCD son los que exhiben menores dimensiones con respecto a los EPZ de eyaculados completos (EE y AV); los parámetros morfométricos tiene variación entre animales. Sin embargo, dada la variabilidad de los parámetros estudiados, se requieren más estudios para entender las implicancias de la diversidad morfométrica sobre la función espermática.
Fuente de financiamiento
Los autores señalan que el presente trabajo fue financiado por el proyecto Estudio, validación y aplicación de biotecnologías reproductivas en el proceso de mejoramiento y valoración genética de alpacas en las provincias de Canas, Canchis y Quispicanchi de la Región del Cusco.
Conflictos de intereses
Los autores señalan que el presente trabajo fue financiado por el proyecto Estudio, validación y aplicación de biotecnologías reproductivas en el proceso de mejoramiento y valoración genética de alpacas en las provincias de Canas, Canchis y Quispicanchi de la Región del Cusco, y no genera conflictos de interés.
Agradecimientos
Esta investigación se desarrolló gracias al proyecto Estudio, validación y aplicación de biotecnologías reproductivas en el proceso de mejoramiento y valoración genética de alpacas en las provincias de Canas, Canchis y Quispicanchi de la Región del Cusco.
Aspectos éticos
Los protocolos utilizados en el estudio se ciñen a las normas Europeas indicada en (https://ec.europa.eu/environment/chemicals/lab_animals/legislation_en.htm para el uso de animales en investigación.
Literatura citada
1. Solís R, editor. Producción de camélidos sudamericanos. Huancayo Perú: Imprenta Ríos; 1997. 550 p. [ Links ]
2. Miragaya M, Martínez Sarrasague M, Casaretto M, Rubin de Celis E, Carretero I, Giuliano S. Assessment of apparent viscosity and analysis of rheological profiles in llama ejaculates. En: 16th International Congress on Animal Reproduction (ICAR); 2008; July 13-17; Budapest. Hungry. [ Links ]
3. Pacheco Curie JI. Métodos de colección de semen en camélidos sudamericanos. Rev Electrón Veterinario 2008;9(5):1-15. [ Links ]
4. Slama R, Eustache F, Ducot B, Jensen TK, Jørgensen N, Horte A, et al. Time to pregnancy and semen parameters: a cross-sectional study among fertile couples from four European cities. Hum Reprod 2002;17(2):503-15. DOI: https://doi.org/10.1093/humrep/17.2.503 [ Links ]
5. Soler C, Gaßner P, Nieschlag E, de Monserrat JJ, Gutiérrez R, Sancho M, et al. Use of the integrated semen analysis system (ISAS®) for morphometric analysis and its role in assisted reproduction technologies. Rev Int Androl 2005;3(3):112-9. DOI: https://doi.org/10.1016/S1698-031X(05)73257-X [ Links ]
6. Partyka A, Niżański W, Ochota M. Methods of assessment of cryopreserved semen. In: Katkov I, editor. Current Frontiers in Cryobiology, Intech Open; 2012. p. 547-74.
7. Nikolettos N, Küpker W, Demirel C, Schöpper B, Blasig C, Sturm R, et al. Fertilization potential of spermatozoa with abnormal morphology. Hum Reprod 1999;14(Suppl 1):S47-70. DOI: https://doi.org/10.1093/humrep/14.suppl_1.47 [ Links ]
8. Menkveld R, Rhemrev JPT, Franken DR, Vermeiden JPW, Kruger TF. Acrosomal morphology as a novel criterion for male fertility diagnosis: relation with acrosin activity, morphology (strict criteria) and fertilization in vitro. Fertil Steril 1996;65(3):637-44. DOI: https://doi.org/10.1016/S00150282(16)58167-9 [ Links ]
9. Gontarz A, Banaszewska D, Gryzińska M, Andraszek K. Differences in drone sperm morphometry and activity at the beginning and end of the season. Turk J Veter Anim Sci 2016;40(5): 598-602. DOI: https://doi.org/10.3906/vet-1511-6 [ Links ]
10. Fumuso FG, Giuliano SM, Chaves G, Neild DM, Miragaya MH, Bertuzzi ML, et al. Incubation of frozen‐thawed llama sperm with seminal plasma. Andrologia 2020;52(6):e13597. DOI: https://doi.org/10.1111/and.13597 [ Links ]
11. Ferrari MR, Spirito SE, Giuliano SM, Fernández HA. Chromatin cytophotometric analysis of abnormal bovine spermatozoa. Andrologia 1998; 30(2):85-9. DOI: https://doi.org/10.1111/j.14390272.1998.tb01151.x [ Links ]
12. Carretero MI, Lombardo D, Arraztoa CC, Giuliano SM, Gambarotta MC, Neild DM. Evaluation of DNA fragmentation in llama (Lama glama) sperm using the sperm chromatin dispersion test. Anim Reprod Sci 2012;131(1-2):63-71. DOI:https://doi.org/10.1016/j.anireprosci.2012.02.008 [ Links ]
13. Soler C, Gadea B, Soler AJ, Fernández Santos MR, Esteso MC, Núñez J, et al. Comparison of three different staining methods for the assessment of epididymal red deer sperm morphometry by computerized analysis with ISAS®. Theriogenology 2005;64(5):1236-43. DOI: https://doi.org/10.1016/j.theriogenology.2005.02.018
14. Yániz JL, Capistrós S, Vicente Fiel S, Soler C, Nuñez de Murga J, Santolaria P. Study of nuclear and acrosomal sperm morphometry in ram using a computer-assisted sperm morphometry analysis fluorescence (CASMA-F) method. Theriogenology 2014;82(6):921-4. DOI: https://doi.org/10.1016/j.theriogenology.2014.06.017 [ Links ]
15. Buendía P, Soler C, Paolicchi F, Gago G, Urquieta B, Pérez Sánchez F, et al. Morphometric characterization and classification of alpaca sperm heads using the sperm-class analyzer computer-assisted system. Theriogenology 2002;57(4): 1207-8. DOI: https://doi.org/10.1016/s0093-691x(01)00724-5 [ Links ]
16. Ordoñez C, Ampuero E, Cucho H, Chalco G. Morphometric characterization of alpaca sperms using the Integrated Sperm Analysis System (ISAS). Spermova 2012;2(1):67-8. DOI: https://doi.org/10.13140/RG.2.1.5169.9449 [ Links ]
17. Soler C, García Molina A, Sancho M, Contell J, Núñez M, Cooper TG. A new technique for analysis of human sperm morphology in unstained cells from raw semen. Reprod Fertil Dev 2016; 28(4):428-33. DOI: https://doi.org/10.1071/RD14087 [ Links ]
18. Evangelista Vargas D, Evangelista Vargas S, Santiani A, Valdivia M. Análisis morfométrico de espermatozoides de alpaca utilizando softwares de captura y medición de imágenes. En: Primer congreso de la Sociedad Latinoamericana de Reproducción Animal; 2015 March 25-28; Buenos Aires. Argentina. [ Links ]
19. Carretero MI, Fumuso FG, Miragaya M, Herrera C, Giuliano SM. Effect of seminal plasma in Lama glama sperm. Reprod Fertility Develop. 2015;27(1):223-223. DOI: https://doi.org/10.1071/RDv27n1Ab267 [ Links ]
20. Carretero MI, Giuliano MS, Neild DM. Evaluation of sperm DNA quality in South American camelids and other domestic species. Spermova 2017;7(1):18-26. DOI: https://doi.org/10.18548/aspe/0005.04 [ Links ]
21. Meza A, Caldeira C, Valverde A, Ordoñez C, Ampuero E, Cucho H, et al. Sperm kinematic characterization of alpaca (Vicugna pacos L.) during the reproductive season. Reprod Domest Anim 2018;53(6):1415-23. DOI: https://doi.org/10.1111/rda.13284 [ Links ]
22. Cucho H, López Y, Caldeira C, Valverde A, Ordóñez C, Soler C. Comparison of three different staining methods for the morphometric characterization of Alpaca (Vicugna pacos) sperm, using ISAS® CASA-Morph system. Nova Biologica Reperta 2019;6(3):284-91. DOI: https://doi.org/10.29252/nbr.6.3.284 [ Links ]
23. Souza T. Avaliação andrológica e criopreservação de sêmen de pumas (Puma concolor Linnaeus, 1771) adultos [tesis maestría]. [Viçosa]: Universidad Federal de Viçosa; 2009 [citado 20 de octubre de 2019]. Recuperado a partir de: https://www.locus.ufv.br/bitstream/handle/123456789/4980/texto%20completo.pdf?sequence=1&isAllowed=y
24. Director A, Giuliano SM, Trasorras V, Carretero MI, Pinto M, Miragaya M. Electroejaculation in llama (Lama glama). J Camel Prac Res 2007; 14(2):203-6. [ Links ]
25. Flores Huarco N, Cucho H, Carretero MI, Ciprián R, Quispe Ccasa HA, Calderón N, Miragaya M, Giuliano SM. Dimethylformamide cryoprotectant effect on cryopreserved alpaca sperm motility (Vicugna pacos) evaluated by analysis system ISAS®. Spermova 2015;5(1):47-50. DOI: https://doi.org/10.18548/aspe/0002.10 [ Links ]
26. García W, Alarcón V, Bravo W. Artificial insemination of alpacas with refrigerated semen and the inclusion of two types of egg yolk. Rev Investig Vet Perú 2017;28(2):337-44. DOI: https://doi.org/10.15381/rivep.v28i2.13080 [ Links ]
27. Vásquez J, Florentini EA, Valdivia M. Hypoosmotic swelling test in alpaca (Vicugna pacos) epididymal spermatozoa. Reprod Domest Anim 2012;47(6):e83-7. DOI: https://doi.org/10.1111/j.1439-0531.2012.01988.x [ Links ]
28. Quispe HA. Funcionalidad de la membrana espermática en semen de alpaca (Vicugna pacos) colectado por desviación de conducto deferente [tesis licenciatura]. [Cusco]: Universidad Nacional de San Antonio Abad del Cusco; 2015. 109 p.
29. Alarcón V, García W, Bravo PW. Artificial insemination of alpacas with semen collected by vaginal aspiration and by artificial vagina. Rev Investig Vet Perú 2012;23(1):58-64. DOI: https://doi.org/10.15381/rivep.v23i1.882 [ Links ]
30. Ordoñez C, Cucho H, Ampuero E, Antezana W, Cayo S. Artificial insemination with fresh, cooled and thawed alpaca semen collected with electroejaculation. Spermova 2013;3(1):65-6. [ Links ]
31. Ciprian Achircana R. Uso de la dimetilformamida en la criopreservación de semen de alpaca (Vicugna pacos) [tesis licenciatura]. [Cusco]: Universidad Nacional de San Antonio Abad del Cusco, Cusco; 2019 [citado 20 de noviembre de 2019]. Recuperado a partir de: http://repositorio.unsaac.edu.pe/handle/UNSAAC/4083
32. Villa N, Castaño D, Duque P, Ceballos A. Glutathione peroxidase and superoxide dismutase activities inblood and seminal plasma in colombian stallions. Rev Colom Cienc Pecua 2012;25(1): 64-70. [ Links ]
33. Novak S, Smith TA, Paradis F, Burwash L, Dyck MK, Foxcroft GR, et al. Biomarkers of in vivo fertility in sperm and seminal plasma of fertile stallions. Theriogenology 2010;74(6):956-67. DOI: https://doi.org/10.1016/j.theriogenology.2010.04.025 [ Links ]
34. Casaretto C, Lombardo DM, Giuliano S, Gambarotta M, Carretero MI, Miragaya MH. Morphometric analysis of llama (Lama glama) sperm head. Andrologia 2012;44(1):424-30. DOI: https://doi.org/101111/j.1439-0272.2011.01200.x [ Links ]
35. Soler C, Sancho M, García Molina A, Núñez J, Parráguez VH, Contell J, et al. Llama and alpaca comparative sperm head morphometric analysis. J Camelid Sci 2014;7:48-58. [ Links ]
36. Giuliano SM, Ferrari MR. Morphometric analysis of head and nuclei of llama spermatozo. Spermova 2015;5(1):110-4. DOI: https://doi.org/10.18548/aspe/0002.25 [ Links ]
37. Flores Huarco NH. Criopreservación de espermatozoides de alpaca (Vicugna pacos) utilizando N, N-dimetilformamida al 4 y 7% [tesis maestría]. [Buenos Aires]: Universidad de Buenos Aires; 2018 [citado 20 de octubre de 2019]. Recuperado a partir de: http://ri.agro.uba.ar/files/download/tesis/maestria/2018floreshuarconilsherber.pdf
38. Meyer RA, Barth AD. Effect of acrosomal defects on fertility of bulls used in artificial insemination and natural breeding. Can Vet J 2001:42 (8);627-34. [ Links ]
39. Zhao L, Burkin HR, Shi X, Li L, Reim K, Miller DJ. Complexin I is required for mammalian sperm acrosomal exocytosis. Dev Biol 2007; 309(2):236-44. DOI: https://doi.org/10.1016/j.ydbio.2007.07.009 [ Links ]
40. Yániz JL, Vicente Fiel S, Capistrós S, Palacín I, Santolaria P. Automatic evaluation of ram sperm morphometry. Theriogenology 2012;77(7):1343-50. DOI: https://doi.org/10.1016/j.theriogenology.2011.10.039 [ Links ]
41. Pizarro E, Restrepo G, Echeverry J, Rojano B. Effect of seminal plasma on the redox state of cryopreserved stallion semen. Rev MVZ Cordoba 2013;18(Suppl 1):3672-80. DOI: https://doi.org/10.21897/rmvz.134 [ Links ]
42. Núñez Martínez I, Morán JM, Peña FJ. Sperm indexes obtained using computer-assisted morphometry provide a forecast of the freezability of canine sperm. Int J Androl 2007;30(3):182-9. DOI. https://doi.org/10.1111/j.1365-2605.2007.00743.x [ Links ]
43. Ball BA, Mohammed HO. Morphometry of stallion spermatozoa by computer-assisted image-analysis. Theriogenology 1995;44(3):367-77. DOI: https://doi.org/10.1016/0093-691x(95)00191-a [ Links ]
44. Lüpold S, Calhim S, Immler S, Birkhead TR. Sperm morphology and sperm velocity in passerine birds. Proc Biol Sci 2009;276(1659):1175-81. DOI: https://doi.org/10.1098/rspb.2008.1645 [ Links ]
45. Bierla JB, Gizejewski Z, Leigh CM, Ekwall H, Söderquist L, Rodriguez Martinez H, et al. Sperm morphology of the Eurasian beaver, Castor fiber: an example of a species of rodent with highly derived and pleiomorphic sperm populations. J Morphol 2007;268(8):683-9. DOI: https://doi.org/10.1002/jmor.10544
46. Malo AF, Gomendio M, Garde J, Lang Lenton B, Soler AJ, Roldan ER. Sperm design and sperm function. Biol Lett 2006;2(2):246-9. DOI: https://doi.org/10.1098/rsbl.2006.0449 [ Links ]
47. Soler C, Sancho M, García A, Fuentes M, Núñez J, Cucho H. Ejaculate fractioning effect on llama sperm head morphometry as assessed by the ISAS® CASA system. Reprod Domest Anim 2014;49(1):71-8. DOI: https://doi.org/10.1111/rda.12226 [ Links ]
48. Giuliano S, Director A, Gambarotta M, Trasorras V, Miragaya M. Collection method, season and individual variation on seminal characteristics in the llama (Lama glama). Anim Reprod Sci 2008;104(2-4):359-69. DOI: https://doi.org/10.1016/j.anireprosci.2007.02.016 [ Links ]
49. Thurston LM, Watson PF, Mileham AJ, Holt WV. Morphologically distinct sperm subpopulations defined by Fourier shape descriptors in fresh ejaculates correlate with variation in boar semen quality following cryopreservation. J Androl 2001;22(3):382-94. DOI: https://doi.org/10.1002/j.1939-4640.2001.tb02194.x [ Links ]
50. Maroto Morales A, Ramón M, García Álvarez O, Soler AJ, Esteso MC, Martínez Pastor F, et al. Characterization of ram (Ovis aries) sperm head morphometry using the Sperm-Class Analyzer. Theriogenology 2010;73(4):437-48. DOI: https://doi.org/10.1016/j.theriogenology.2009.10.003
51. Maree L, du Plessis SS, Menkveld R, van der Horst G. Morphometric dimensions of the human sperm head depend on the staining method used. Hum Reprod 2010;25(6):1369-82. DOI: https://doi.org/10.1093/humrep/deq075 [ Links ]
52. Hirai M, Boersma A, Hoeflich A, Wolf E, Foll J, Aumüller TR, et al. Objectively measured sperm motility and sperm head morphometry in boars (Sus scrofa): Relation to fertility and seminal plasma growth factors. J Androl 2001;22(1):104-10. DOI: https://doi.org/10.1002/j.1939-4640.2001.tb02159.x [ Links ]
53. Banaszewska D, Andraszek K, Szostek M, Wójcik E, Danielewicz A, Walczak Jędrzejowska R. Analysis of stallion semiologic semen parameters. Med Weter 2015;71(9):563-7. [ Links ]
54. Banaszewska D, Andraszek K, Zdrowowicz E, Danielewicz A. The effect of selected staining te chniques on stallion sperm morphometry. Livest Sci 2015;175:128-32. DOI: https://doi.org/10.1016/j.livsci.2015.02.017 [ Links ]
55. Hidalgo M, Rodríguez I, Dorado J, Soler C. Morphometric classification of Spanish thoroughbred stallion sperm heads. Anim Reprod Sci 2008;103(1-3):374-8. DOI: https://doi.org/10.1016/j.anireprosci.2007.06.001 [ Links ]
56. Walczak Jedrzejowska R, Marchlewska K, Oszukowska E, Filipiak E, Bergier L, Slowikowska Hilczer J. Semen analysis standardization: is there any problem in Polish laboratories? Asian J Androl 2013;15(5):616-21. DOI: https://doi.org/10.1038/aja.2013.48 [ Links ]
57. Banaszewska D, Andraszek K, Czubaszek M, Biesiada Drzazga B. The effect of selected staining techniques on bulls sperm morphometry. Anim Reprod Sci 2015;159:17-24. DOI: https://doi.org/10.1016/j.anireprosci.2015.06.019 [ Links ]
58. Kondracki S, Banaszewska D, Wysokińska A, Iwanina M. The effect of sperm concentration in the ejaculate on morphological traits of bull spermatozoa. Folia Biol (Krakow) 2012;60(1-2): 85-91. DOI: https://doi.org/10.3409/fb60_1-2.85-91 [ Links ]
59. Núñez Martínez I, Moran JM, Peña FJ. Sperm indexes obtained using computer-assisted morphometry provide a forecast of the freezability of canine sperm. Int J Androl 2007;30(3):182-9. DOI: https:/doi.org/10.1111/j.1365-2605.2007.00 743.x [ Links ]
60. Andraszek K, Szeleszczuk O, Niedbała P, Kuchta Gładysz M. Preliminary research on evaluation of sperm morphometry and chromatin structure in the semen of silver fox (Vulpes vulpes). Folia Pomeranea Univ Technol Stetin Agric., Alimento Piscaria Zootech 2016;326(38)2:5-16. DOI: https://doi.org/10.21005/AAPZ2016.38.2.01
61. Brito LF, Greene LM, Kelleman A, Knobbe M, Turner R. Effect of method and clinician on stallion sperm morphology evaluation. Therigenology 2011;76(4):745-50. DOI: https://doi.org/10.1016/j.theriogenology.2011.04.007 [ Links ]
______________
Nota del Editor:
Journal of the Selva Andina Animal Science (JSAAS) se mantiene neutral con respecto a los reclamos jurisdiccionales publicados en mapas y afiliaciones institucionales.











 texto en
texto en 
 uBio
uBio 



